Nos processos químicos industriais, muitas vezes trabalha-se
com substâncias gasosas em etapas com reações
químicas, mudança de fase ou transporte, por exemplo.
Dessa maneira, faz-se necessário o entendimento das
propriedades dos gases.
Face ao exposto, assinale a alternativa correta.
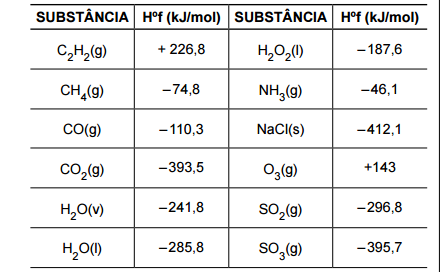
Dentre os gases do efeito estufa que estão aumentando
de concentração, podem ser citados o dióxido de carbono
e o metano. Sabe-se que a quantidade de metano
emitida é bem menor, mas seu potencial de aquecimento
é cerca de 21 vezes superior ao do dióxido de carbono.
Nesse sentido, um pesquisador sugeriu que o metano
fosse queimado como forma de atuar no problema. Com
base nos dados de calores de formação a 25 ºC, assinale
a alternativa que indica corretamente o calor de reação
da combustão do metano em kJ/mol.
Uma das maneiras de enunciar a 1°Lei da Termodinâmica
é: “a variação da energia do sistema tem que ser igual
à energia transferida através das suas fronteiras com as
vizinhanças". Assim, para um sistema fechado sem reação química, ela pode ser expressa pela equação:
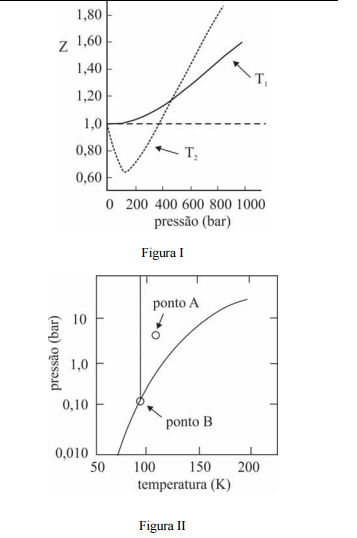
A figura I ilustra o gráfico do coeficiente de compressibilidade (Z)
do CH4 (g) em função da pressão para duas temperaturas distintas
(T1 e T2), e a figura II representa o diagrama de fases desse mesmo
composto. A partir das figuras apresentadas, julgue os itens que se
seguem.
Na temperatura e pressão correspondentes ao ponto A da
figura II, o potencial químico do metano gasoso é superior ao
do metano líquido.
Com relação às misturas de vapor d'água com ar atmosférico em
determinada temperatura ambiente e volume fixo, julgue os itens
subsequentes.
Em determinadas condições, é possível que 100 g de água
estejam contidos em 1,0 kg de ar úmido a 25 °C.
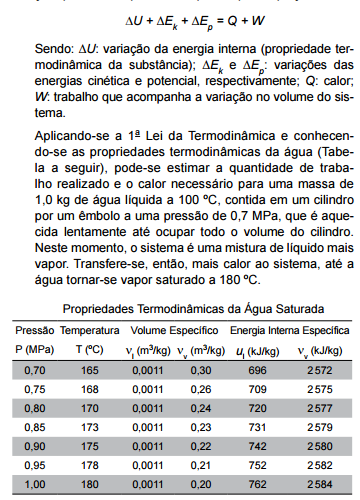
Uma empresa, diante da elevação dos preços da energia
elétrica e das descobertas de grandes reservas de gás de xisto nas
proximidades de suas instalações, resolveu investir na geração
própria de energia termoelétrica. O gás de xisto é composto
principalmente por metano (CH4), cuja equação de combustão é
CH4 (g) + 2O2 (g) –> CO2 (g) + 2H2O (l). A tabela a seguir mostra
os dados termodinâmicos, a 25 ºC, relativos aos compostos
envolvidos na equação apresentada.
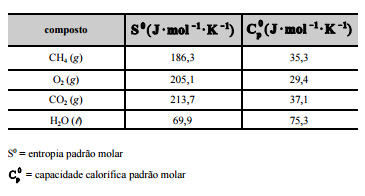
Com relação a essa situação hipotética, julgue os itens
subsequentes, considerando que a combustão do CH4 ocorra de
forma completa; que a entalpia padrão de combustão do CH4 (g), a
25 ºC, seja igual a –890 kJ/mol; e que as massas molares, em g/mol,
do C, do H e do O sejam iguais a 12,0, 1,0 e 16,0, respectivamente.
Considerando–se um comportamento ideal para a mistura sob
pressão total p, é correto afirmar que, em uma amostra de gás
natural constituída por 95%, em massa, de metano e, o restante,
de etano, a pressão parcial do metano será superior a 0,95p.

A figura I ilustra o gráfico do coeficiente de compressibilidade (Z)
do CH4 (g) em função da pressão para duas temperaturas distintas
(T1 e T2), e a figura II representa o diagrama de fases desse mesmo
composto. A partir das figuras apresentadas, julgue os itens que se
seguem.
O CH4 não pode ser liquefeito por simples compressão à
temperatura de 150 K, uma vez que o ponto B, na figura II,
corresponde à temperatura crítica desse gás.
Com relação às misturas de vapor d'água com ar atmosférico em
determinada temperatura ambiente e volume fixo, julgue os itens
subsequentes.
Se a temperatura de bulbo úmido e a de bulbo seco forem
iguais, então o ar estará saturado, não sendo necessária a carta
psicrométrica para estimar a umidade relativa.

A figura I ilustra o gráfico do coeficiente de compressibilidade (Z)
do CH4 (g) em função da pressão para duas temperaturas distintas
(T1 e T2), e a figura II representa o diagrama de fases desse mesmo
composto. A partir das figuras apresentadas, julgue os itens que se
seguem.
Infere–se da situação mostrada na figura I que T1 é maior que
T2.
Uma empresa, diante da elevação dos preços da energia
elétrica e das descobertas de grandes reservas de gás de xisto nas
proximidades de suas instalações, resolveu investir na geração
própria de energia termoelétrica. O gás de xisto é composto
principalmente por metano (CH4), cuja equação de combustão é
CH4 (g) + 2O2 (g) –> CO2 (g) + 2H2O (l). A tabela a seguir mostra
os dados termodinâmicos, a 25 ºC, relativos aos compostos
envolvidos na equação apresentada.

Com relação a essa situação hipotética, julgue os itens
subsequentes, considerando que a combustão do CH4 ocorra de
forma completa; que a entalpia padrão de combustão do CH4 (g), a
25 ºC, seja igual a –890 kJ/mol; e que as massas molares, em g/mol,
do C, do H e do O sejam iguais a 12,0, 1,0 e 16,0, respectivamente.
A combustão de um mol de CH4 (g), em condições padrão a
25 ºC, gera uma redução de mais de 1.000 kJ na energia livre
de Gibbs do sistema.

A figura I ilustra o gráfico do coeficiente de compressibilidade (Z)
do CH4 (g) em função da pressão para duas temperaturas distintas
(T1 e T2), e a figura II representa o diagrama de fases desse mesmo
composto. A partir das figuras apresentadas, julgue os itens que se
seguem.
Na temperatura T2, o CH4 (g), a 200 bar de pressão, ocupará
um volume superior ao estimado pela equação dos gases ideais,
o que demonstra que as forças atrativas predominam sobre as
forças repulsivas.
Com relação às misturas de vapor d'água com ar atmosférico em
determinada temperatura ambiente e volume fixo, julgue os itens
subsequentes.
Em uma carta psicrométrica, as linhas de umidade relativa
constante se afastam à medida que a temperatura de bulbo seco
aumenta.
Observe, a seguir, o diagrama de fases quando duas substâncias estão misturadas e aquecidas, como ocorre, por exemplo, num processo de destilação simples.
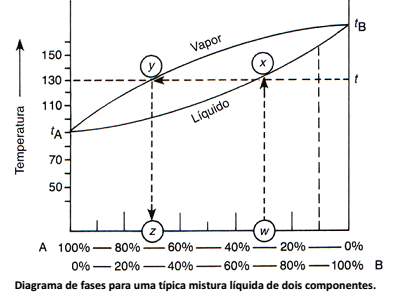
De acordo com o diagrama apresentado, analise as afirmativas.
I. Mostra o comportamento de uma mistura de dois líquidos numa destilação simples; as linhas horizontais representam temperaturas constantes. A curva superior representa a composição do vapor e a curva inferior se refere à composição do líquido.
II. Para qualquer temperatura constante (linha horizontal), como, por exemplo, a linha t, a intersecção da linha com as curvas dão as composições do líquido e do vapor durante a destilação, que estão em equilíbrio entre si, naquela temperatura t.
III. No diagrama observa‐se que à temperatura t, a intersecção da curva em x indica que o líquido da composição w estará em equilíbrio com o vapor da composição z, que corresponde à intersecção em y.
IV. O diagrama mostra que, teoricamente, a destilação simples não poderia ser usada para separar A e B, pois sempre haverá a mistura de A e B em qualquer temperatura, e só haveria 100% de A puro em tA (esquerda do diagrama) e 100% de B puro em tB (direita do diagrama). Entretanto, é possível fazer uma separação aceitável da mistura de A e B, por destilação simples, em seus componentes relativamente puros, se a diferença entre os pontos de ebulição de A e B for maior do que 100°C.
Estão corretas as afirmativas
Analise o seguinte diagrama de fases quando duas substâncias estão misturadas e aquecidas, como ocorre, por exemplo, num processo de destilação fracionada.

Diante do exposto, assinale a afirmativa INCORRETA.
Aenergia livre de Gibbs é uma propriedade de estado
utilizada na análise de equilíbrio e espontaneidade de
reações. Sobre esse tópico é correto afirmar que:

