O carbonato de magnésio (um sal) é aquecido para produzir o óxido de magnésio (um óxido básico), que, ao reagir com água, forma o hidróxido de magnésio. A partir do sal, produziu-se o hidróxido de magnésio em duas etapas (ver reações), cada uma com rendimento percentual de 90%.

A massa de Mg(OH)2 obtida a partir de uma massa inicial de MgCO3 igual a 2,1 g é
A decomposição do carbonato de cálcio é representada por:
CaCO 3 (s) → CaO (s) + CO2 (g)
Considerando as massas molares dos elementos carbono,
oxigênio e cálcio, respectivamente, iguais a 12 g mol−1,
16 g mol−1 e 40 g mol−1, julgue o item a seguir.
Na decomposição completa de 50 g de carbonato de cálcio, obtém-se um resíduo sólido de CaO de massa igual a 28 g.
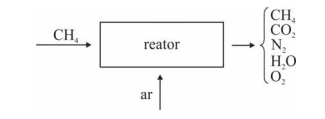
Em um reator ideal, de processo contínuo, que opera em
estado estacionário, a combustão de CH4 ocorre com uma
conversão de 90% do reagente limitante. Esse reator é alimentado
com CH4 e ar a taxas de 16 kg/h e 300 kg/h, respectivamente,
conforme ilustrado no esquema apresentado.
Considerando que, nessa situação, a combustão do CH4 seja
completa e que a composição do ar que alimenta o reator seja de
24%, em massa, de O2 (g) e, o restante, de N2 (g), julgue o item
subsequente.
A porcentagem, em massa, de CO2 na corrente de saída do
reator é superior a 10%.
Acerca dos processos físicos que ocorrem por difusão de massa,
julgue os itens seguintes.
Em geral, a conservação de massa total requer que o somatório
dos fluxos difusivos de todas as espécies seja maior que um.
Um analista produziu uma solução aquosa quando diluiu 2 x 103 µg de certa enzima com massa molecular igual a 28.000 Da (aproximadamente 28.000 u), em 1 cm3 de água. Em seguida, realizou um ensaio enzimático, adicionando 100 x 10–3 mL da solução da enzima em um recipiente que já continha uma mistura contendo 290 µL de um tampão adequado (pH 8) e mais 10 µL do substrato da enzima (concentração igual a 2 x 10–3 mols/L). As concentrações molares finais (no ensaio enzimático) da enzima e do substrato enzimático são, respectivamente,


