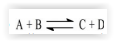Os alquenos são matéria-prima de grande importância na indústria porque podem ser facilmente transformados em uma vasta gama de compostos químicos. Exemplos típicos são as reações de hidratação e de polimerização catalisadas por ácido. Com relação às reações de alquenos, julgue o item subsequente.
O efeito da adição do catalisador ácido é o de reduzir a energia de ativação da reação e, com isso, aumentar a fração de colisões efetivas.
A velocidade é constante e não depende da concentração dos reagentes. Não existe uma relação direta entre os coeficientes e a ordem da reação. Essas são características cinéticas de reação de
A equação
descreve a reação entre dois
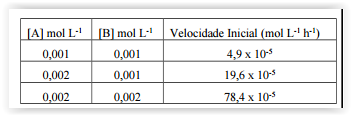
gases cuja avaliação é mencionada na tabela que se segue.
De acordo com os dados apresentados, a constante de
velocidade nessa reação, em mol-3 L3 h-1, é:
A reação em fase gasosa a A + b B → c C + d D foi estudada em diferentes condições de concentração inicial dos reagentes, tendo sido obtidos os seguintes resultados experimentais, todos na mesma temperatura:
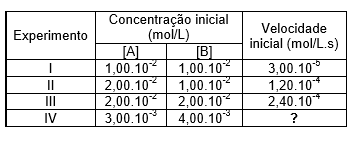
A partir dos dados experimentais da tabela, indique a alternativa que apresenta o valor correto da velocidade inicial da reação no experimento IV.
A reação: (CH3)3CCl + OH- → (CH3)3COH + Cl- foi estudada em solução aquosa e o mecanismo proposto é:

Para esse processo podemos afirmar que:
O ácido fluorídrico (HF(aq.)) é utilizado na gravação de vidro, pois esse composto reage com o SiO2 segundo as seguintes
reações:
SiO2(s) + 4HF(aq.) → SiF4(g) + 2H2O(l) (Equação I)
SiO2(s) + 6HF(aq.) → H2[SiF6](aq.) + 2H2O(l) (Equação II)
Devido à toxidez do SiF4(g), qual das ações a seguir poderIa evitar a formação desse composto no pr°Cesso descrito?
A realização de aulas experimentais de química é uma importante estratégia para o ensino de cinética química. No tocante ao estudo da relação existente entre a superfície de contato dos reagentes e a velocidade da reação química, o procedimento experimental que melhor expressa essa relação é:
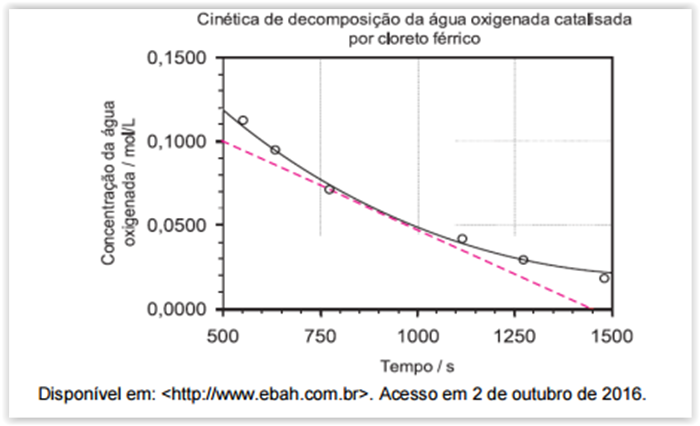
Considere o gráfico a seguir.
O gráfico expressa a cinética de decomposição da água oxigenada catalisada por
cloreto férrico. Por meio desse gráfico, verifica-se que a
Sabendo que o carbono grafite sofre combustão segundo a equação abaixo e que a velocidade de formação do dióxido de carbono é 4 mol/minuto.
C(grafite) + O2(g) CO2(g)
Assinale a alternativa que apresenta a velocidade de consumo do gás oxigênio.
Estudos cinéticos da reação 2NO + O2 → 2 NO2 mostraram que quando a concentração inicial de O2 é dobrada e a concentração de NO é mantida constante, a velocidade da reação dobra; quando a concentração inicial de NO é dobrada e a de O2 é mantida constante, a velocidade inicial quadruplica. Qual será o incremento da velocidade inicial da reação quando as concentrações iniciais de O2 e de NO forem triplicadas?