A solução de Cloreto de Sódio 0,9% é amplamente utilizada em laboratórios. Foi solicitado ao técnico de laboratório que prepare 700 mL dessa solução. Qual massa de Cloreto de Sódio deve ser utilizada para preparar o volume solicitado?
A acidez de uma solução é definida pela concentração de íons H+. Considerando-se essa afirmação, assinale a alternativa que corresponde a uma substância capaz de transformar uma solução ácida em uma solução básica.
O oxigênio é abundante na atmosfera, mas pouco solúvel na água, constituindo-se no fator do meio mais limitante para a produção de peixes em cativeiro. Sobre a solubilidade do oxigênio dissolvido na água de viveiros escavados utilizados para piscicultura, é correto afirmar que
Dispõe-se em estoque de um frasco contendo HC2H3O2 concentrado (massa molar 60,05 g·mol-1, densidade 1,05 g·cm-3 e % p/p 99,5) e deseja-se preparar 1 litro de solução 0,1N desse ácido. O volume, em mL, do ácido concentrado que deve ser utilizado no preparo dessa solução é
As quantidades máximas de oxigênio molecular gasoso e de água líquida que podem ser produzidas na reação de decomposição de 1 litro de uma solução aquosa 0,4 mol.L-1 de peróxido de hidrogênio é:
Quanto ao processo de dissolução que ocorre com o estabelecimento de novas interações entre soluto e solvente, assinale a alternativa correta.
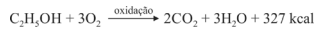
Sabendo que a reação apresentada mostra o processo de oxidação do etanol — em que são liberadas 327 kcal por mol de energia — e que as massas atômicas do carbono, do oxigênio e do hidrogênio são, respectivamente, iguais a 12, 16 e 1, julgue o item a seguir.
Álcool etílico hidratado é uma mistura homogênea.
No processo de dissolução de um soluto molecular em um líquido, as forças de atração entre as moléculas do soluto e do solvente devem ser
A respeito de soluções e concentração de soluções, julgue o item a seguir.
O tipo de composição porcentual de um reagente sempre deve estar especificado explicitamente. O erro potencial resultante de uma opção incorreta é considerável. Por exemplo, para uma solução de hidróxido de sódio comercial a 50% (m/m), sua concentração corresponde a 50% (m/v) de hidróxido de sódio.
Uma amostra de carbonato de sódio (Na
2CO3) impuro de 5,00 g foi totalmente dissolvida em 500 mL de ácido clorídrico (HC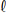
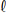
Considerando que a solubilidade do acetato de sódio é igual a 123,5g / 100g de água a 20°C, no que se refere à dissolução do soluto, é correto afirmar que
A respeito de soluções e concentração de soluções, julgue o item a seguir.
As três formas de expressar a concentração em termos de porcentagem, a saber, porcentual em massa, porcentual em volume e porcentual em massa/volume, apresentam a característica de serem independentes da temperatura.
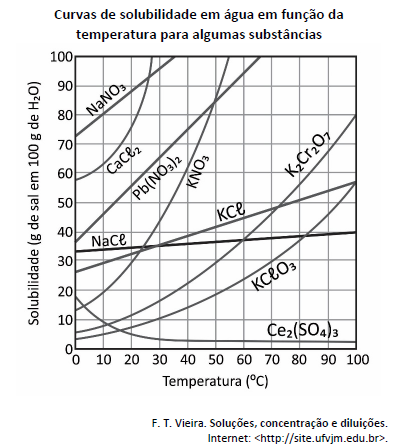
A substância presente no gráfico que apresenta dissolução exotérmica é o
A precipitação de cátions metálicos pela adição de um ânion com o qual eles formem composto insolúvel é uma ferramenta bastante utilizada para a remoção, identificação e(ou) quantificação de um metal em solução. Por exemplo, a adição de uma solução de H 2S é empregada para promover a precipitação de sulfetos metálicos pouco solúveis.
Considerando que as constantes de ionização ácida do H
2S (Ka1 e Ka2) sejam iguais a 1,0 × 10-7 e 1,0 × 10-13, que o produto de solubilidade (Kps) do CdS seja igual a 1,0 × 10-27 e que todas as soluções envolvidas apresentem comportamento ideal, julgue o item a seguir.
A massa de H2S presente em 250 mL de uma solução aquosa com concentração 0,100 mol/L do ácido é superior a 1,0 g.
Alguns reagentes específicos podem ser empregados na identificação de drogas ilícitas, por meio da formação de produtos coloridos e rapidamente identificáveis a olho nu, como o reagente de Marquis, empregado para identificar metanfetaminas; o reagente de Scott, usado para identificar cocaína; e o reagente de Simons, usado para discriminar entre anfetaminas e metanfetaminas. Tendo o texto precedente como referência inicial, julgue o item subsecutivo, relativo a aspectos diversos pertinentes a química analítica.
O volume de formaldeído 45% (densidade = 0,815 g × cm!3; massa molar = 30,031 g mol!1) necessário para se preparar 100 mL de uma solução de concentração 1,0 mol L!1 é superior a 82 mL.