Em relação à espectrometria de massas, foram
feitas as seguintes afirmativas:
I. Analisadores de massas de alta resolução podem
distinguir íons de compostos diferentes que
tenham a mesma massa molecular nominal.
II. Apenas analisadores de massas de alta resolução
podem apresentar dois íons para o mesmo
fragmento de fórmula CnHmCl.
III. O espectro de massas de um composto contendo
carbonos, hidrogênios e dois átomos de bromo
em sua molécula, independente da resolução do
equipamento, apresentará picos distantes duas
unidades de m/z um do outro e contendo a
mesma área.
IV.Independente da resolução do espectrômetro,
será observado para o íon molecular do item III
um pico central distante duas unidades de m/z de
dois picos laterais com a metade de sua área.
Assinale a alternativa correta:
As análises quantitativas a nível traço são bastante requeridas em determinações por espectrometria de massas. Entre as afirmações nas seguintes alternativas, assinale a INCORRETA:
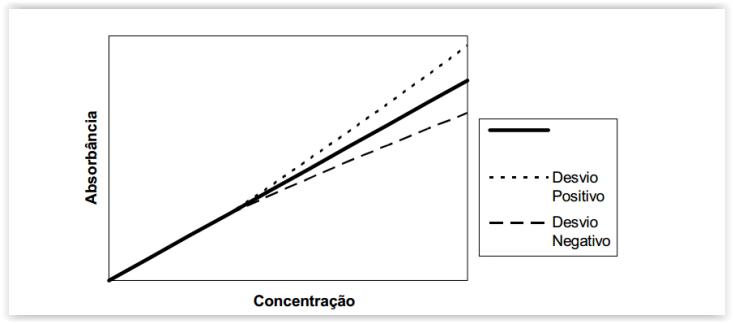
Os desvios por limitação da Lei de Lambert-Beer são aqueles que as interações
do analito com o solvente e demais solutos variam com o aumento da
concentração. Observe o gráfico abaixo e assinale quais afirmativas são
VERDADEIRAS.
I. Em soluções concentradas do analito ou outros solutos, as interações soluto-soluto
alteram a estrutura do analito e também modificam a sua absortividade.
II. Ao ocorrer um desvio na Lei de Lambert-Beer ainda pode-se trabalhar com a curva de
calibração, embora ela não seja uma reta.
III. Como os desvios normalmente ocorrem em concentrações muito baixas, uma das
soluções mais comuns é a pré-concentração.
IV. Os desvios são positivos e negativos conforme as alterações aumentem ou diminuam
a absorvidade.
V. Os desvios podem ser químicos ou causados pela instrumentação, entretanto, neste
último, o desvio é praticamente nulo, devido a equipamentos de alta tecnologia.
Sobre os erros em análises químicas, os
parâmetros estatísticos utilizados para as suas
avaliações e os conceitos de exatidão e precisão,
julgue os itens abaixo com V para VERDADEIRO
ou F para FALSO.
I - A exatidão descreve a reprodutibilidade das
medidas, em outras palavras, a proximidade
entre os resultados que foram obtidos através de
réplicas autênticas.
II - O desvio-padrão, a variância e o coeficiente
de variação são função de quanto os resultados
individuais diferem da média e são amplamente
empregados para descrever a precisão de um
conjunto de dados de réplicas.
III - Em geral, os erros grosseiros ocorrem de
forma ocasional, são grandes e levam a erros
absolutos negativos.
IV - Os erros aleatórios, ou indeterminados,
afetam a precisão dos resultados, enquanto os
erros sistemáticos, ou determinados, afetam a
exatidão dos resultados.
Uma análise química consiste na determinação dos componentes de uma amostra. Quando o objetivo é isolar e identificar os compostos químicos (elementos, íons, moléculas...), denomina-se análise qualitativa. Assinale a alternativa INCORRETA.
A técnica de precipitação é amplamente utilizada na química analítica. Os métodos gravimétricos são quantitativos e se baseiam em medidas de massa. Sobre a gravimetria, todas as alternativas estão corretas, EXCETO:
Assinale a alternativa que apresenta a correta explicação da importância de se considerar a temperatura como um parâmetro de qualidade da água.
“Existe grande número de caminhos possíveis para percorrer as etapas em uma análise quantitativa. No exemplo mais simples, ______________, adquirimos e processamos a amostra, dissolvemos a amostra em um solvente apropriado, medimos uma propriedade do analito e estimamos a____________. Dependendo da complexidade da amostra e do método escolhido, várias outras etapas podem ser necessárias”. Assinale a alternativa que corresponde as palavras CORRETAS para cada respectivo espaço vazio.
O fluxograma a seguir sumariza os resultados obtidos por um
técnico na pesquisa de cátions do grupo I.
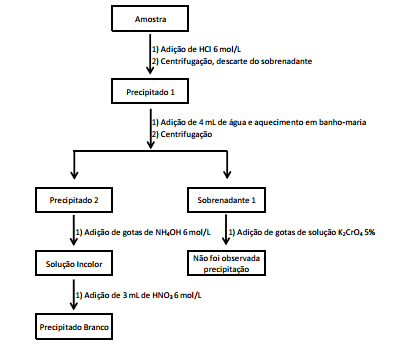
A análise deste fluxograma permite concluir que, na amostra,
possivelmente está presente o cátion
A acidez do vinho é expressa em termos da concentração de
ácido tartárico, cuja fórmula estrutural é representada abaixo.
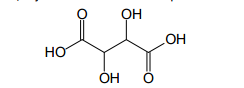
Para a determinação da acidez, 25,00mL de amostra de vinho
branco foram transferidos para Erlenmeyer. Adicionou-se 100mL
de água e gotas de fenolftaleína e titulou-se contra solução
padronizada de NaOH 0,100mol.L-1 Foram necessários 20,00mL
de solução da base na titulação.
A acidez da amostra (em unidades de gramas de ácido
tartárico/100mL) é:
Dado: Massa molar do ácido tartárico: 150g.mol-1
O teor de Ca2+ em amostra de urina foi determinado a partir das
seguintes etapas:
1- Precipitação do cátion por adição de excesso de solução
padrão de C2O42-
0,010 mol.L-1 a 5,00 mL de amostra de urina.
2- Lavagem do precipitado com água gelada para remoção do
oxalato livre e ressolubilização do sólido com solução ácida.
3- Titulação do H2C2O4 em solução utilizando solução padrão de
MnO
Após tratamento do precipitado, foram gastos 15,00 mL de
solução de MnO4- para a titulação do H2C2O4
A concentração de Ca2+ na amostra, em mol.L-1, é
Uma amostra de K2SO4 comercial, contaminada com KCl, foi
submetida a um ensaio gravimétrico para a determinação de sua
pureza. Assim, 1,148g da amostra foi dissolvido em água e
tratada com solução de Ba(NO3)2 O precipitado, após os cuidados
necessários, foi pesado sendo observada a massa 1,398g.
O teor de K2SO4 na amostra é
Dados: Massas molares K24 = 174g.mol–1 KCl= 74,5g.mol–1
BaSO4 = 233g.mol–1
Um material de referência, certificado para fluoreto em 1,06mg.L1, foi analisado em um laboratório por três metodologias
diferentes. Foram analisadas 6 réplicas em cada método
analítico.
As médias dos resultados (em mg.L–1) são apresentados a seguir:
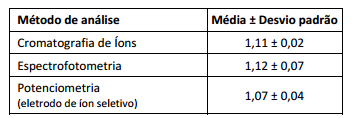
Analisando os resultados, é correto afirmar que o método
O indicador metalocrômico conhecido como negro de eriocromo T é empregado na análise de cálcio por
Uma amostra de 100,0 mL de água teve a concentração de íons cloreto determinada através da reação contra uma solução padrão de nitrato de prata. Sabe-se que uma alíquota de 10,00 mL da amostra, ao reagir com excesso de nitrato de prata, formou 287,0 mg de precipitado.
A concentração de íons cloreto, em mol.L-1, presente na amostra de água, é de