Uma amostra de 15,0 g de bronze (liga metálica de cobre
e estanho) foi completamente dissolvida com ácido nítrico
concentrado, resultando em 1,00 L de solução aquosa.
Um volume de 0,500 L dessa solução foi misturado com
excesso de ferrocianeto de potássio, também em solução,
formando 17,0 g de um precipitado de ferrocianeto de cobre,
conforme a reação apresentada a seguir.
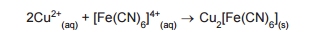
Sabendo-se que o Sn2+ não forma produto sólido com
o íon ferrocianeto, sendo apenas um íon espectador, a
massa de cobre, em g, presente na amostra de bronze é,
aproximadamente
Dados: M(Cu2 [Fe(CN)6 ] (s)) = 339 g mol-1 M(Cu) = 63,5 g mol-1
