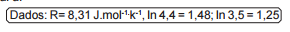Diariamente, inúmeras situações mostram a infl uência da
temperatura na rapidez com que as reações químicas se processam.
Por exemplo, a efervescência de um comprimido antiácido é
maior em água à temperatura ambiente do que em água gelada.
Os alimentos são colocados na geladeira, pois uma diminuição
da temperatura faz com que a decomposição dos alimentos por
micro–organismos ocorra de forma mais lenta. Em um experimento,
a constante de velocidade (k) para a decomposição de primeira
ordem de um composto em solução foi determinada a várias temperaturas
(T), conforme mostra a tabela a seguir:
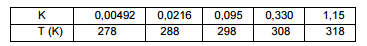
A energia de ativação para a reação de decomposição pode ser
calculada a partir da tabela e seu valor, em kJ.mol–1, é aproximadamente
igual a: