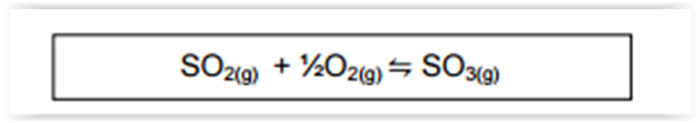O fenômeno de corrosão metálica causa grandes prejuízos às indústrias, pois nesse
processo ocorre a dissolução lenta da superfície de equipamentos, quando os mesmos são expostos ao ar,
em contato com o solo ou água do mar. Com o objetivo de minimizar a corrosão do ferro em equipamentos,
são utilizados os chamados “eletrodos de sacrifício", os quais são formados por barras de outros metais,
convenientemente escolhidos que, quando colocados em contato com a superfície do equipamento, sofrem
corrosão no lugar do ferro
Com base nos dados tabelados, são considerados “eletrodos de sacrifício" adequados as barras de
Uma das etapas possíveis de formação da chuva ácida pode ser representada pelo
equilíbrio
A expressão da constante de equilíbrio KC, com base na lei de ação das massas, para esta reação é
Um volume de 10,00 mL de uma amostra aquosa de Y foi transferido com uma pipeta
volumétrica para um balão volumétrico de 100,00 mL, o qual teve seu volume ajustado até a marca de
aferição com água destilada, de modo a se ter uma solução de trabalho. Essa solução foi analisada por
Espectrofotometria UV-vis e apresentou um valor de absorbância ( A ) de 0,600 em 240 nm e caminho óptico
de 1 cm. A curva de calibração construída para a análise dessa amostra possui a seguinte equação: A =0,030C, onde C é a concentração de Y, em mg L-1
, na solução. A concentração, em mg L-1, do composto Yna amostra é
Os álcoois são compostos versáteis, e podem ser usados como material de partida para a preparação de uma grande variedade de produtos. A reação de oxidação parcial de um álcool secundário, cuja fórmula geral é dada por R2CHOH, gera como produto um(a)
O número de maneiras de dividir 12 pessoas em 3 grupos de 4 pessoas cada é igual a
No sistema de juros compostos, à taxa de juros de 10% ao mês, o número de meses em que deve ser aplicado um capital de R$10.000,00 para que a aplicação renda juros de R$ 4.641,00 é igual a
Um reservatório com capacidade de 500 litros continha 50 litros de água ao meio-dia de um certo dia. A partir desse instante, despejou-se água no reservatório de modo que o volume de água nele passou a aumentar a uma razão constante de q litros por hora. Às 16 horas daquele dia, o volume de água no reservatório era igual a 100 litros. O volume de água no reservatório, em litros, às 19 horas daquele dia era igual a
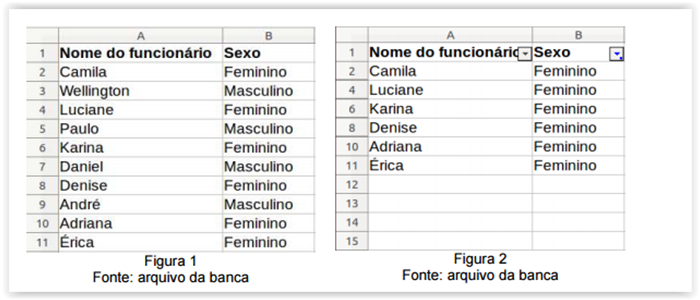
Uma nova planilha foi criada, utilizando-se o LibreOffice Calc 4.2. Nas colunas A e B foram
inseridas informações (nome e sexo) de funcionários de uma empresa fictícia. O resultado é mostrado na
figura 1 abaixo. O LibreOffice Calc 4.2 oferece algumas funcionalidades para manipulação de planilhas
como, por exemplo, as descritas a seguir.
I.Classificar Dados. Exemplo: selecione as colunas A e B, clique no menu “Dados", em seguida na
opção “Classificar" e, finalmente, clique OK.
II.Autofiltro. Exemplo: selecione as colunas A e B, clique no menu “Dados", em seguida abra o submenu
“Filtro" e clique na opção “Autofiltro".
III.Filtragem. Exemplo: após criação do Autofiltro, clique sobre o botão que aparece no canto inferior
direito da célula B1, desmarque o valor “Masculino" e clique em OK.
IV.Ocultar Linhas. Exemplo: para as linhas 3, 5, 7 e 9, uma de cada vez, posicione o ponteiro do mouse
sobre a junção do cabeçalho da linha com a linha seguinte, clique e arraste para diminuir sua altura,
soltando assim que a mensagem “Ocultar" for exibida.
Dentre os recursos e exemplos descritos anteriormente, os que precisam ser usados para, a partir da figura
1, ter como resultado a figura 2, acima, são
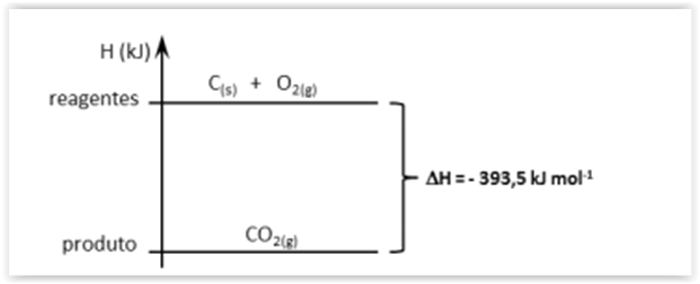
A reação de 1 mol de grafita, C(s), com 1 mol de oxigênio gasoso produz 1 mol de dióxido
de carbono gasoso. O diagrama abaixo mostra a variação de entalpia para essa reação.
Analise as afirmativas abaixo sobre essa reação.
I.A energia liberada pode ser chamada de entalpia de formação de CO2(g).
II.A energia liberada pode ser chamada de entalpia de combustão de grafita.
III.É uma reação endotérmica.
IV.Para queimar 1 mol de C(s), é necessário fornecer 393,5 kJ para o sistema.
Está(ão) CORRETA(S):
O volume de água adicionado a 50 mL de solução de hidróxido de sódio (NaOH), cuja concentração é igual a 60 g L-1 , para que seja obtida uma solução a 5,0 g L-1 , será
Uma amostra de 6,000 g de hematita, um mineral de ferro, foi dissolvida completamente em
ácido, e o ferro presente foi totalmente reduzido a Fe2+. A seguir, a amostra dissolvida foi transferida para
um balão volumétrico de 250,0 mL, o qual foi completado com água destilada até a marca de aferição. Uma
alíquota de 10,00 mL dessa solução contendo o Fe2+ foi titulada com exatamente 25,00 mL de uma solução
padrão 0,020 mol L-1
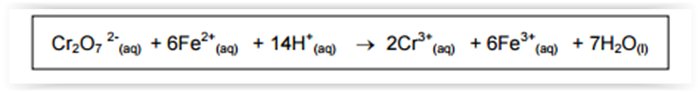
de dicromato, em meio ácido, segundo a equação abaixo.
Considerando a estequiometria dessa reação, a porcentagem em massa de Fe na amostra analisada é,
aproximadamente, igual a
A técnica de espectroscopia de absorção na região do UV/visível é um método óptico de análise baseado na Lei de Beer-Lambert, a qual relaciona a absorção da radiação pelas moléculas do analito com a concentração do mesmo. Sobre a Lei de Beer-Lambert, considere as afirmações que se seguem: I.A absorbância (A ) de uma solução está relacionada com a transmitância de forma logarítmica, A=-log T. II.A absorbância é diretamente proporcional à concentração de uma espécie absorvente (c) e ao caminho óptico (b ) do meio absorvente, A=?bc. III.A constante de proporcionalidade chamada absortividade molar, à qual é dado o símbolo especial ?, é independente da natureza da espécie analisada. IV.Se a concentração é expressa em mols por litro e o caminho óptico em centímetros, então o coeficiente de absortividade molar possui as unidades de L moL-1cm-1 . Estão corretas APENAS as afirmativas
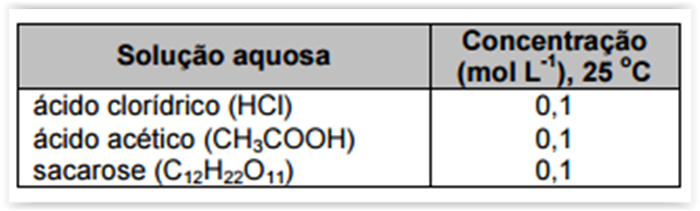
A técnica de condutometria direta pode avaliar o comportamento de soluções aquosas
quanto à condução de corrente elétrica, por meio de medidas de condutância. Essa condutância é um
resultado da soma da contribuição individual de cada íon presente na solução. A tabela a seguir mostra
diferentes tipos de soluções aquosas e suas concentrações.
Considerando as medidas de condutância que poderiam ser obtidas para essas soluções, é CORRETO
afirmar:
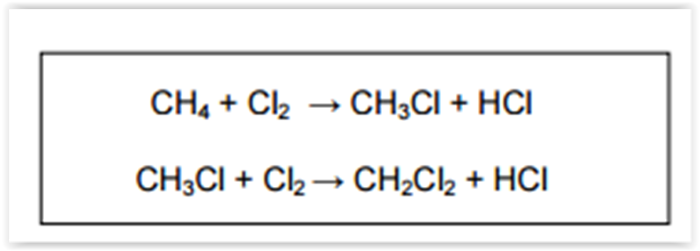
A obtenção do diclorometano (CH2Cl2), um solvente orgânico utilizado na indústria química,
ocorre em duas etapas. Na primeira etapa, o clorometano (CH3Cl) é produzido devido à reação entre o
metano (CH4) e o gás cloro. Na segunda etapa, o clorometano produzido reage com gás cloro formando o
diclorometano. Essas reações ocorrem em temperatura adequada na presença de luz e em um mesmo
reator.
As reações mostradas acima para a obtenção de diclorometano são de
Em uma empresa, ? 350 funcionários leem pelo menos uma das revistas A e B; ? 20 funcionários leem a revista A, mas não leem a revista B; ? 10% dos funcionários que leem a revista B também leem a revista A. O total de funcionários da empresa que leem a revista B, mas não leem a revista A, é igual a