Em 1989, um adolescente em Ohio foi envenenado com vapor de mercúrio derramado. O
nível de mercúrio determinado em sua urina, que é proporcional a sua concentração no
organismo, foi de 1,54 mg.L–1 . O Hg2+ é eliminado do organismo por um processo de
primeira ordem que tem meia–vida de 6 dias (6D).
Após 30 dias (30D), se medidas terapêuticas não fossem tomadas, é CORRETO afirmar
que a expressão matemática que deduzirá a concentração de Hg2+ na urina do paciente,
em mg L–1 será
As cadeias de átomos de carbono de compostos orgânicos podem chegar a
comprimentos muito grandes e dar origem a macromoléculas. Os polímeros são
compostos macromoleculares, em que redes de unidades repetitivas pequenas formam
moléculas gigantes.
Numere COLUNA II de acordo com a COLUNA I, relacionando o tipo de polimerização e
o monômero gerador do polímero.

Assinale a alternativa que apresenta a sequência CORRETA.
A acrilonitrila é empregada na síntese de fibras acrílicas (poliacrilonitrilas). Sua estrutura
química é a seguinte:
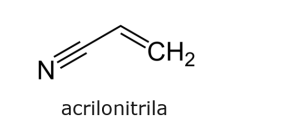
Com relação a essa estrutura, um químico descreveu sobre os orbitais híbridizados de
cada átomo de carbono da acrilonitrila no sentido da esquerda para a direita.
No sentido indicado, é CORRETO afirmar que os orbitais hibridizados dos átomos de
carbono são, respectivamente:
Na titulação de neutralização de 20,00 mL de ácido acético (CH3COOH) 0,100 mol/L com
10,00 mL de solução de NaOH 0,200 mol/L, é CORRETO afirmar que o pH da solução
titulada será aproximadamente igual a
Considere que Ka = 1,8×10–5; log2 = 0,3; log3 = 0,5
Considere os seguintes compostos: GeO44–; K4Ge4Te10 e Ca4GeO5.
Os números de oxidação do germânio nos compostos citados são, respectivamente:
Os elementos do bloco d da tabela periódica têm suas propriedades intermediárias entre
os elementos do bloco s e os do bloco p, o que explica a denominação para esses
elementos de metais de transição.
Sobre esses metais, assinale a alternativa INCORRETA.
O excesso em massa de iodeto de sódio (NaI) foi adicionado a 50 mL de uma solução de
AgNO3 e formou–se um precipitado de 1,5 g de AgI.
Nessas condições, é CORRETO afirmar que a concentração inicial da solução de AgNO3
é aproximadamente, de
Em 1910, Ernest Rutherford e colaboradores executaram o famoso experimento com
partículas radioativas.
A respeito do experimento proposto por Rutherford é CORRETO afirmar que o que
conduziu seu experimento a propor um novo modelo atômico com núcleo pequeno e
denso foi o fato de que
O ozônio, embora benéfico na estratosfera, em que forma uma camada protetora contra
efeitos danosos da radiação ultravioleta, tem efeitos tóxicos nas camadas mais baixas da
atmosfera, por afetar diretamente os seres vivos. A molécula de ozônio consiste na sua
estrutura distâncias O–O iguais.
Sobre a molécula de ozônio e sua estrutura química, assinale com V as afirmativas
verdadeiras e com F as falsas.
( ) Para descrever adequadamente a estrutura do ozônio, escrevemos duas
estruturas de Lewis e indicamos que a molécula real é descrita pela média das
duas estruturas de ressonância.
( ) A estrutura de Lewis da molécula de ozônio é constituída por um ciclo que requer
ligações simples O–O de iguais energias de ligação.
( ) A estrutura de Lewis da molécula de ozônio consiste em moléculas lineares com
duas distâncias O–O iguais.
( ) A molécula de ozônio tem duas ligações O–O equivalentes, cujos comprimentos
são intermediários entre os comprimentos das ligações simples e dupla.
Assinale a alternativa que apresenta a sequência CORRETA.
O azobenzeno é um corante orgânico usado em muitas aplicações, como tingir tecidos.
Muitas tinturas azo são derivadas da substância orgânica C12H10N2. A fórmula estrutural
plana do azobenzeno está representada a seguir.
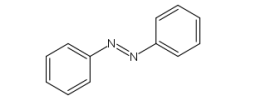
Sobre o azobenzeno, foram feitas as seguintes afirmativas:
I. A hibridizações nos átomos de nitrogênio são do tipo sp2.
II. O orbital 2p do nitrogênio exerce superposição frontal, produzindo uma ligação TT.
III. Cada átomo de carbono possui um orbital 2p não hibridizado.
A partir dessas observações, conclui–se que estão CORRETAS as afirmativas:
Um estudante de eletrônica foi preparar uma solução de cloreto férrico (FeCl3) para
corroer uma placa de circuito. Para isso, preparou 2 mol/L de solução de FeCl3 em um
balão volumétrico de 100 mL.
Considerando–se a solução de cloreto férrico preparada, qual a quantidade de mol de
cobre foi corroída se metade da quantidade de matéria de FeCl3 foi consumida no
processo de corrosão?
O fluoreto de lítio (LiF) é um sólido iônico que apresenta a estrutura cristalina igual à do
cloreto de sódio (NaCl). Veja a estrutura do NaCl abaixo:
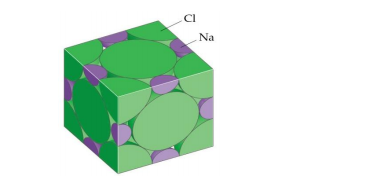
Considere que, hipoteticamente, os raios iônicos do Li+
e do F–são, respectivamente, 0,08 nm e 0,10 nm.
Sobre a estrutura cristalina do fluoreto de lítio, é CORRETO afirmar que
Considere que um químico recebeu uma solução para analisar se há a presença dos íons
Ag+, Ca2+ e/ou Hg2+. Os testes em sequência feitos pelo químico e os resultados obtidos
foram:
I. Adicionou à solução ácido clorídrico, e nada aconteceu.
II. Adicionou ácido sulfúrico diluído e formou–se um precipitado branco.
III. Filtrou o sólido e adicionou sulfeto de hidrogênio na solução residual e formou–se um
precipitado preto.
A partir das análises feitas pelo químico e seus resultados, é CORRETO afirmar que os
íons presentes na solução são
São espécies utilizadas como nucleófilos em uma reação de substituição nucleofílica,
EXCETO:
Considere as moléculas abaixo:
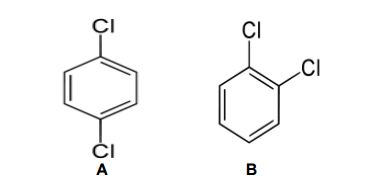
Analise as comparações realizadas entre as duas moléculas citadas.
I. A molécula B é o o–dicloro–benzeno e ela tem temperatura de ebulição mais baixa.
II. A molécula A é o p–dicloro–benzeno e ela tem polaridade mais baixa.
III. As moléculas A e B são isômeros de posição.
A partir dessa análise, conclui–se que estão CORRETAS.

