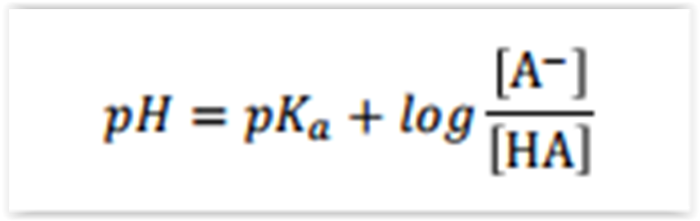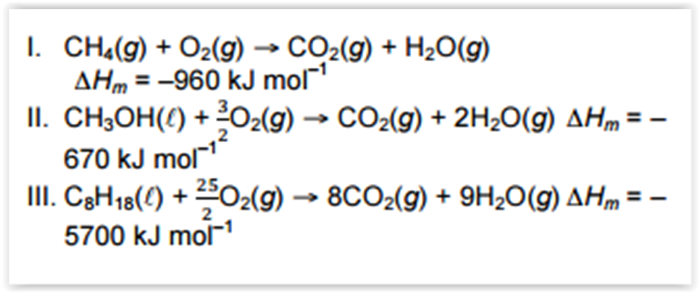Responder numerando corretamente a questão da
coluna da direita, que descreve a finalidade do uso
de EPIs e outros cuidados pessoais que devem ser
observados para proteção individual, de acordo com
a coluna da esquerda, que apresenta a
classificação dos mesmos:
1.Cabelos preferencialmente mantidos presos ou sob gorros
2.Guarda-pó
3.Luvas de
procedimentos
4.Óculos
5.Restrições ao uso
de joias ou similares
6.Sapatos fechados
( ) Evitar danos nos materiais nobres mediante processo oxidação
( ) Evitar o contato com material biológico ou químico durante a manipulação de materiais e uso de equipamentos
( ) Proteção dos olhos contra respingos e resíduos de vidros ou outros materiais
( ) Proteção dos pés quanto a impactos e derramamentos de líquidos corrosivos
( ) Proteção quanto à manipulação de reagentes diversos
( ) Proteção quanto à manipulação de reagentes, equipamentos e procedimentos laboratoriais
A alternativa que contém a sequência correta dos
números da coluna da direita, de cima para baixo, é:
Para que os resíduos de laboratório possam ser eliminados de forma adequada, é necessário ter à disposição recipientes de tipo e tamanho adequados. Os recipientes coletores devem ser caracterizados claramente de acordo com o seu conteúdo, o que também implica em se colocar símbolos de periculosidade. No caso de embalagem para resíduos químicos perigosos, pode-se afirmar que: I.Resíduos líquidos contendo solventes devem ser armazenados em garrafas de vidro ou bombonas de material compatível. II.Resíduos líquidos isentos de solventes devem ser armazenados em frascos metálicos ou de aço inoxidável. III.Resíduos sólidos e lodos devem ser armazenados em recipientes (embalagens) individuais resistentes à ruptura. Assinale a alternativa correta:
Uma solução tampão é definida como uma solução
de um par de ácido-base conjugado ou uma base-
ácido conjugado. Essa solução tem a capacidade
de resistir a variações de pH quando são
adicionadas pequenas quantidades quer de ácido,
quer de base. As soluções tampões são muito
importantes nos sistemas químicos e biológicos. O
pH de uma solução tampão pode ser estimado pela
equação de Henderson-Hasselbalch:
imagem
em que, o HA é o ácido e A– é a base conjugada.
Com base no exposto, identifique as afirmativas
verdadeiras.
I.O pH da solução será igual ao pKa se a [A–] forigual a [HA]
II.O pH tende a aumentar se a concentração a [A–]for maior que [HA]
III.O pH tende a diminuir se a concentração a [A–]for maior que [HA]
IV.O pH tende a aumentar se a concentração a [A–]for menor que [HA]
V.O pH tende a diminuir se a concentração a [A–]for menor que [HA]
Assinale a alternativa correta:
A palavra cinética, no caso da Química, refere-se à
velocidade de uma reação, isto é, à variação da
concentração de desaparecimento de um reagente
ou de surgimento de um produto com o tempo. Para
exemplificar, considere que a 280 °C, o dióxido de
nitrogênio se decompõe no óxido nítrico e oxigênio:
2NO 2(g ) → 2NO(g ) + O2(g )
E que em um experimento, a concentração de NO 2
diminui de 0,010 mol L –1 a 0,005 mol L–1
no período de
100 s. Qual é a velocidade média de desaparecimento
de NO2?
Nos Estados Unidos (USA), os postos de
combustíveis automotivos geralmente
disponibilizam gás (CH4, metano), metanol (CH3OH,
álcool metílico) e gasolina (C8H18, fórmula química
aproximada), respectivamente. A reação de
combustão completa e energia liberada na forma de
calor desses combustíveis são apresentadas a
seguir:
Com base nos dados estabeleça a ordem
decrescente dos combustíveis em relação a energia
liberada com uma mesma quantidade em massa.
No laboratório, principalmente de Química, o acondicionamento de soluções ácidas e básicas deve ser uma prática adequada e correta, para evitar alteração na composição e outros danos. Das alternativas a seguir, indique a forma CORRETA de acondicionamento de solução de ácido sulfúrico e de solução de ácido fluorídrico, respectivamente:
Relacione o tipo de resíduo químico (coluna à esquerda)
com o respectivo exemplo (coluna à esquerda):
Tipo de Resíduos
Químicos
I. Básicos
II. Metais preciosos ou recicláveis
III. Oxidantes fortes
IV. Redutores fortes (exceto metais e ligas)
V. Solventes descartáveis
VI. Solventes recicláveis
Exemplo
( ) Soluções ou sais de dicromato, permanganato, hipoclorito, iodato, persulfato, bismuto (III). Solução de bromo, iodo, peróxido de idrogênio. Sólidos: bismutato de sódio, dióxido de chumbo e ácido crômico.
( ) Cabeça e cauda de destilação, solvente de limpeza, solventes contaminados de difícil purificação e misturas azeotrópicas.
( ) Hidrazina, soluções ou sais de sulfito, iodeto, tiossulfato, oxalato, ferro (II), estanho (II) e fósforo vermelho.
( ) Aminas, soluções de hidróxidos, soda cáustica, solução alcoolato e amônia.
( ) Solventes de HPLC, extração Sohxlet e rotaevaporados, e formol.
( ) Sais ou soluções contendo prata, ósmio, ouro, platina e rutênio.
Assinale a alternativa com a sequência CORRETA
de cima para baixo:
As variações de entalpia que ocorrem durante as reações químicas com frequência têm o mesmo interesse prático que as relações de massas, pois, no caso das reações de combustão, que envolvem combustíveis como o gás natural e petróleo, são realizadas cotidianamente mais pela energia térmica que liberam do que pelos seus produtos da combustão. Por exemplo, a combustão de 1,00 mol de metano, CH4, produz dióxido de carbono e água e libera 802 kJ mol–1 . Quando 3,00 mol de oxigênio reagem com uma quantidade estequiométrica de metano, qual é ?H para a reação?
Devido à grande emissão de gases lançados na
atmosfera, nas regiões mais populosas é evidente a
ocorrência da chuva ácida. Na sua precipitação, um
dos ácidos responsáveis pela acidez é o sulfúrico.
Um equilíbrio envolvido na formação desse ácido na
água da chuva está representado pela equação:
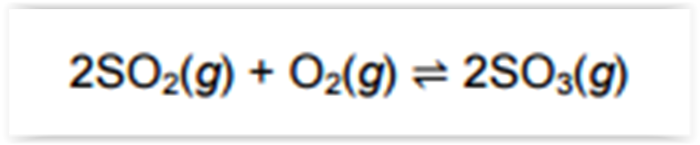
Considere que são colocados 6 mol de SO2, 5 mol
de O 2 e 4 mol de SO3 num recipiente fechado de 5,0 L
para reagirem até o sistema atingir o equilíbrio a dada
temperatura. A variação do número de mol dos gases
participantes está registrada no gráfico.
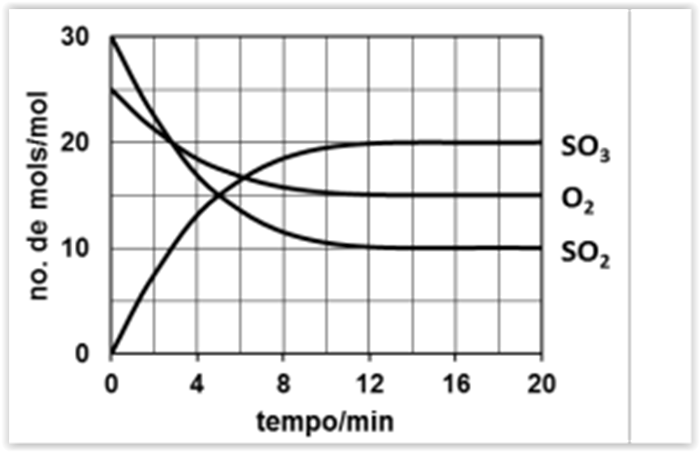
Nestas condições, a constante de equilíbrio, KC, é igual a:
Existem muitos motivos para estudar a velocidade
de uma reação, do ponto de vista prático, o
conhecimento das velocidades de reações é útil na
concepção de medicamentos, no controle da
poluição e no processamento de alimentos, bem
como nas aplicações de setores produtivos em
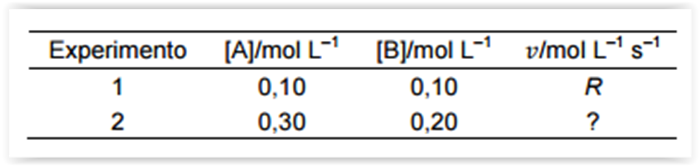
geral. Então para exemplificar, considere que a
velocidade de uma reação entre os compostos A e
B segue a lei de velocidade,
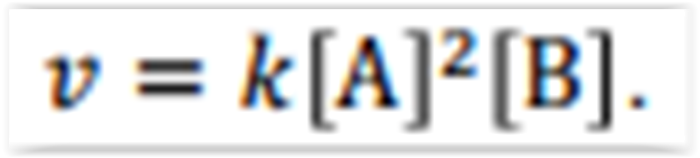
velocidade do Experimento 2 observada a mesma
temperatura do Experimento 1.