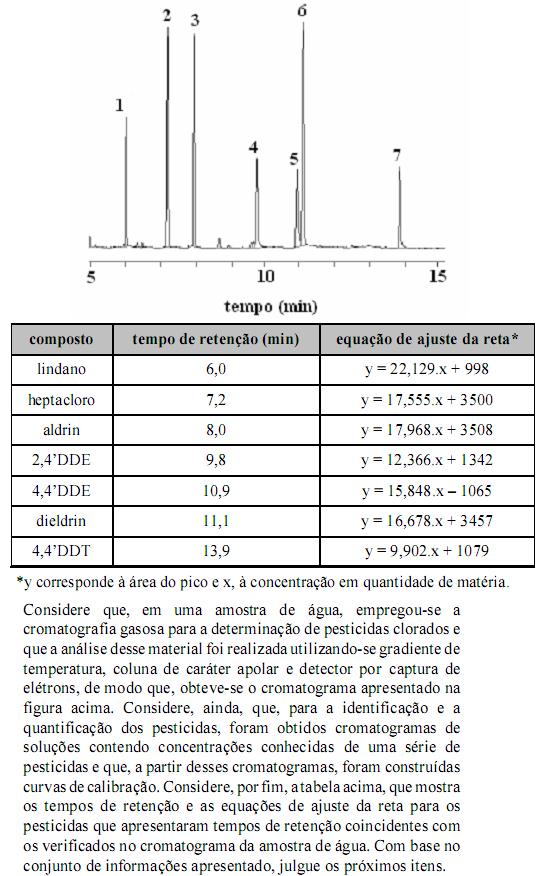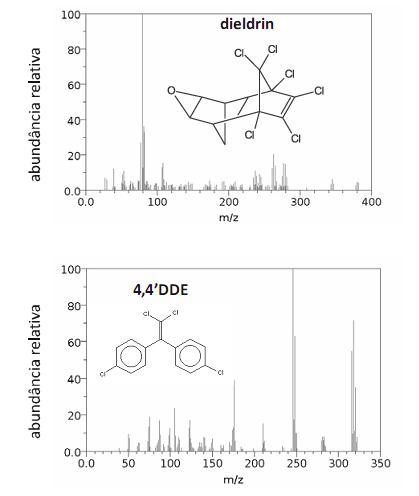
Os espectros de massa mostrados acima são, respectivamente, do dieldrin e do 4,4DDE, compostos que usualmente têm seus picos parcialmente sobrepostos em cromatogramas. Considere, ainda, que o elemento cloro apresenta massa molar igual a 35,5 g/mol e apenas dois isótopos, com números de massa iguais a 35 e 37. A partir dessas informações, julgue os itens que se seguem.
A porcentagem do isótopo do cloro com número de massa 35 é maior que 70%.
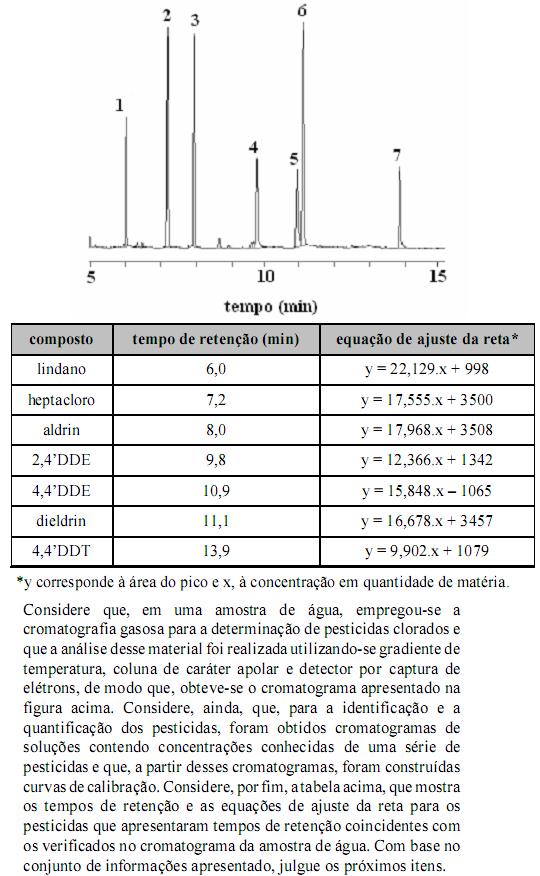
A análise cromatográfica da amostra acima pode ser realizada, sem prejuízos à identificação e à quantificação dos compostos, substituindo-se o detector por captura de elétrons por um detector por ionização em chama.
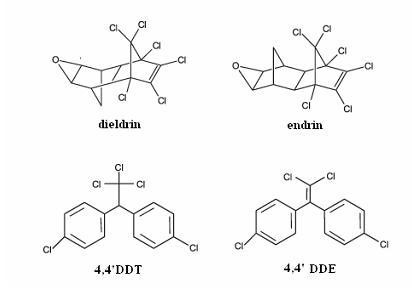
Considerando a figura acima, que ilustra as estruturas químicas de quatro pesticidas, julgue os itens que se seguem.
O composto 4,4DDE consiste no principal produto da reação do 4,4DDT com KOH, que se processa via mecanismo de eliminação bimolecular.
Preparou-se 100 mL de uma solução padrão de biftalato de potássio, de acordo com o seguinte procedimento: (i) pesagem de um béquer vazio em uma balança analítica; (ii) pesagem do béquer contendo 2,0000 g do biftalato na mesma balança; (iii) dissolução do biftalato, por meio da adição de água suficiente ao béquer; (iv) transferência de todo o conteúdo do béquer para um balão volumétrico de 100,00 mL; (v) preenchimento do balão com água até o menisco.
Considerando as informações acima e que os desvios padrão sejam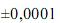 g, para uma simples leitura na balança utilizada, e
g, para uma simples leitura na balança utilizada, e 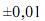 mL, para uma leitura de menisco no balão, julgue os próximos itens.
mL, para uma leitura de menisco no balão, julgue os próximos itens.
O desvio padrão relativo para a concentração da solução de biftalato de potássio preparada é maior que 1,0×10-4 .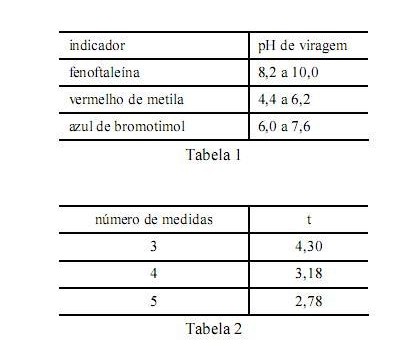
Considere que uma solução de NaOH foi padronizada por meio da titulação, em quadruplicata, com 20,00 mL de uma solução padrão de biftalato de potássio 0,1000 mol/L e que a concentração média encontrada para a solução de NaOH foi de 0,080 mol/L, com uma estimativa do desvio padrão de ±0,002 mol/L. Considere, ainda, a tabela 1, em que é apresentado o pH de viragem de alguns indicadores ácido-base, e a tabela 2, em que são apresentados os valores do parâmetro t de student para uma probabilidade de 95%.
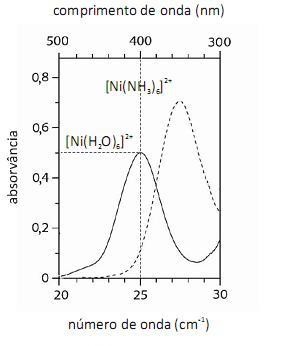

De acordo com a lei de Beer, infere-se do espectro do complexo 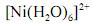 que, para uma radiação com comprimento de onda igual a 400 nm, a absortividade molar é maior que
que, para uma radiação com comprimento de onda igual a 400 nm, a absortividade molar é maior que 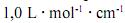 .
.
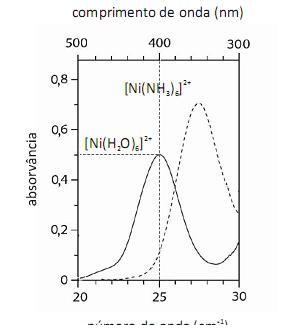

A análise espectroscópica do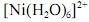 mostra que a razão entre o número de fótons com comprimento de onda igual a 400 nm que atinge o transdutor e o número desses fótons que atinge a amostra é maior do que 0,40.
mostra que a razão entre o número de fótons com comprimento de onda igual a 400 nm que atinge o transdutor e o número desses fótons que atinge a amostra é maior do que 0,40.

Com base no conjunto de informações acima, julgue os itens que se seguem, referentes aos equilíbrios e às espécies.
A constante de equilíbrio K pode ser calculada por meio da expressão K = 
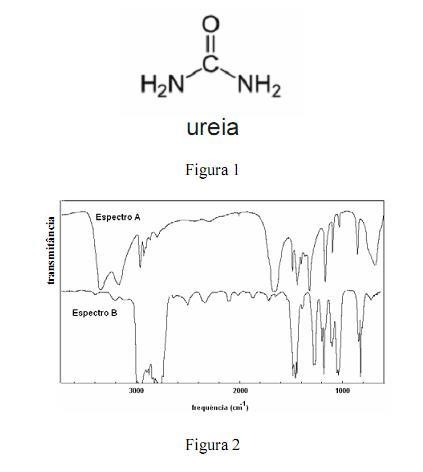
A amônia serve como substrato para a síntese de um grande número de substâncias, como aminas e amidas. Merece destaque a ureia, que é largamente empregada como fertilizante e cuja estrutura é apresentada na figura 1. Na figura 2, são apresentados os espectros de infravermelho de duas outras substâncias que podem ser sintetizadas a partir da amônia: a propanamida e a trietilamina, sendo que os espectros não estão apresentados, necessariamente, nessa ordem. Com relação aos derivados da amônia citados e aos espectros apresentados, julgue os itens que se seguem.
A reação da amônia com a propanona resulta na formação da etanamida.
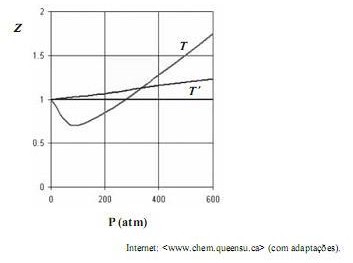
Considerando que, sob pressões elevadas, os gases deixam de apresentar comportamento ideal, e que a figura acima apresenta as curvas do coeficiente de compressibilidade (Z) para o 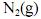 em duas temperaturas distintas (T e T'), julgue os itens subsequentes.
em duas temperaturas distintas (T e T'), julgue os itens subsequentes.
A temperatura T é superior à temperatura T.
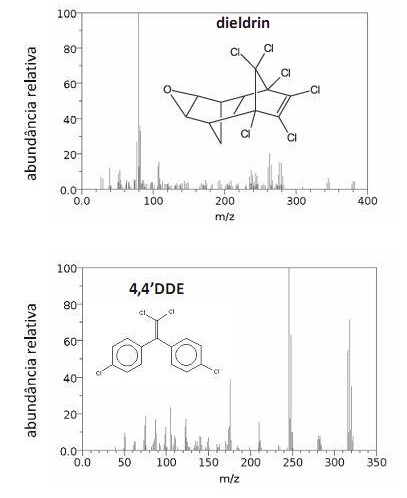
Os espectros de massa mostrados acima são, respectivamente, do dieldrin e do 4,4DDE, compostos que usualmente têm seus picos parcialmente sobrepostos em cromatogramas. Considere, ainda, que o elemento cloro apresenta massa molar igual a 35,5 g/mol e apenas dois isótopos, com números de massa iguais a 35 e 37. A partir dessas informações, julgue os itens que se seguem.
No espectro de massa do 4,4DDE, o pico em m/z igual a 116 corresponde a um íon molecular do composto.
Considerando-se a fase estacionária da coluna utilizada, é correto afirmar que o composto correspondente ao pico 7 apresenta maior ponto de ebulição que o composto correspondente ao pico 1.
A extração com solvente apolar ou de baixa polaridade consiste em uma técnica eficiente para a extração de compostos orgânicos a partir de soluções aquosas. Define-se o coeficiente de partição (K) como a razão entre as concentrações do composto no solvente orgânico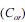 e na fase aquosa
e na fase aquosa 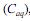 , quando atingido o
, quando atingido o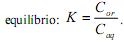
Dois estudantes realizaram a extração de um composto, a partir de uma solução aquosa com a concentração do composto igual a 0,0100 mol/L. O estudante A realizou uma única extração, utilizando 100 mL da solução aquosa e 100 mL de 1-octanol, e o estudante B utilizou o mesmo volume da solução aquosa, mas realizou duas extrações consecutivas, cada uma com 50 mL de 1-octanol.
Considerando o conjunto de informações apresentado acima e que o coeficiente de partição do composto no sistema 1-octanol/água seja igual a 2,0, julgue os itens que se seguem.
A fração do composto extraída pelo estudante B será maior que a extraída pelo estudante A.
Preparou-se 100 mL de uma solução padrão de biftalato de potássio, de acordo com o seguinte procedimento: (i) pesagem de um béquer vazio em uma balança analítica; (ii) pesagem do béquer contendo 2,0000 g do biftalato na mesma balança; (iii) dissolução do biftalato, por meio da adição de água suficiente ao béquer; (iv) transferência de todo o conteúdo do béquer para um balão volumétrico de 100,00 mL; (v) preenchimento do balão com água até o menisco.
Considerando as informações acima e que os desvios padrão sejam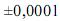 g, para uma simples leitura na balança utilizada,
g, para uma simples leitura na balança utilizada,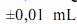 e , para uma leitura de menisco no balão, julgue os próximos itens.
e , para uma leitura de menisco no balão, julgue os próximos itens.
Caso a solução de biftalato preparada seja usada, posteriormente, na padronização de uma solução básica, a presença de impurezas no biftalato usado para a preparação de sua solução gerará um erro aleatório que, consequentemente, afetará a precisão dos resultados obtidos durante a padronização.
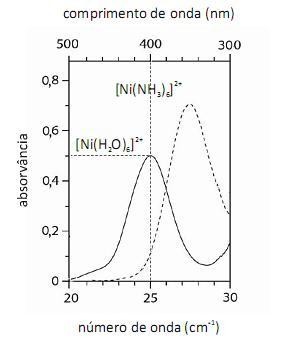

O fato de os espectros acima apresentarem largas bandas de absorção, em vez de linhas ou picos estreitos, demonstra que o equipamento utilizado não possuía monocromador.
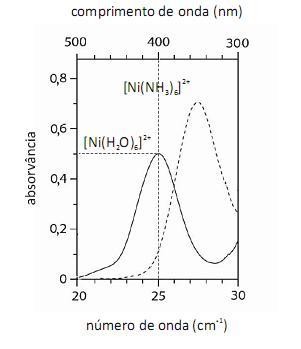

Em face dos espectros acima apresentados, é correto concluir que o módulo do valor da energia de estabilização do campo cristalino (EECC) para o complexo 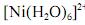 é superior a 4,0×10-19 J.
é superior a 4,0×10-19 J.