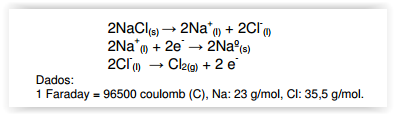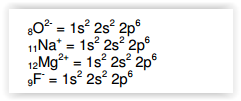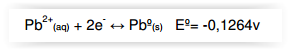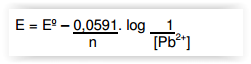No jornal Folha de São Paulo, de 12 de agosto
de 2012, foi publicada uma reportagem sobre a
droga sintética ecstasy ´´[...] Um levantamento inédito
feito pela Superintendência da Polícia Técnico-Científica
de São Paulo em parceria com a Fapesp revela que
apenas 44,7% das drogas sintéticas apreendidas no
Estado no último ano contêm o princípio ativo do
ecstasy, o MDMA […]".
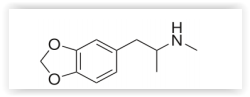
Considere a fórmula estrutural plana da MDMA.
Baseado nas informações fornecidas e nos conceitos
químicos, analise as afirmações a seguir.
l A molécula de MDMA possui fórmula molecular
C11H15NO2.
ll Na molécula de MDMA existe o fenômeno da mesomeria.
lll A molécula de MDMA possui a função química
amida.
lV A molécula de MDMA possui ao menos um carbono
assimétrico.
Todas as afirmações corretas estão em:
Na eletrólise ígnea do cloreto de sódio ocorre a
formação de sódio metálico e gás cloro após a
fusão do NaCl(s).
Qual massa de sódio metálico e o volume de
gás cloro na CNTP produzidos após 2,5 minutos
de eletrólise sob uma corrente de 10 A?
Com relação aos conceitos sobre pH e pOH,
analise as afirmações a seguir.
l O produto iônico da água (Kw) não é alterado pela
temperatura.
ll A 25ºC, uma solução aquosa apresenta uma concentração
de íons [H+
] = 7.10-5 mol/L. O pOH dessa
solução é 9,8 sendo essa solução ácida.
lll Indicadores ácido-base geralmente são ácidos
fracos nos quais moléculas (HIn) e ânions (In-)
apresentam cores diferentes.
lV Considere o xampu (pH = 8) e o café (pH = 5). A
concentração dos íons H+ do café é três vezes
maior que a do xampu.
Dado: log7 = 0,8
Todas as afirmações corretas estão em:
Considere a distribuição eletrônica das espécies
químicas abaixo.
Assinale a alternativa que representa a ordem
crescente do raio iônico das espécies químicas
acima:
DNA e RNA são biopolímeros. O DNA é sintetizado
a partir de desoxinucleotídeos e o RNA
por nucleotídeos.
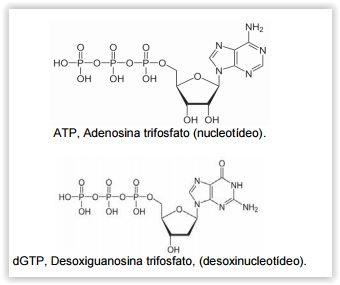
Considere a fórmula estrutural plana de dois
tipos de moléculas que são utilizados na síntese
desses biopolímeros:
Baseado nas informações fornecidas e nos conceitos
químicos, analise as afirmações a seguir.
l Ambas as moléculas possuem a função química
amida em sua estrutura.
ll Na molécula ATP, não existem elétrons p em ressonância.
lll Ambas as moléculas possuem ao menos uma
amina terciária
lV Na molécula dGTP existe uma carbonila.
Todas as afirmações corretas estão em:
Com relação aos conceitos sobre equilíbrios
químicos, analise as afirmações a seguir.
l Alterando a concentração dos participantes de um
equilíbrio químico, Kc não altera, mas poderá
ocorrer a variação do α.
ll Alterando a temperatura de um equilíbrio químico,
Kc é alterado, assim como α.
lll Em um equilíbrio químico a adição de um catalisador
não altera Kc assim como α.
lV Nos equilíbrios que envolvem gases, uma altera-
ção na pressão total não altera Kc nem Kp mas
varia α.
Dados:
Kc = constante de equilíbrio em função da concentração dos
participantes em mol/L.
Kp = constante de equilíbrio em função da pressão parcial dos
participantes gasosos.
α = grau de dissociação do equilíbrio (%).
Todas as afirmações corretas estão em:
Qual a energia liberada na combustão completa
de 138g de CH3CH2OH(l), a 25ºC e 1 atm?
Dados: Entalpias de formação das substâncias a 25ºC e 1
atm: CH3CH2OH(l) = - 278 kJ/mol; CO2(g) = - 394 kJ/mol; H2O(g)
= - 242 kJ/mol. C: 12 g/mol, O: 16 g/mol, H: 1 g/mol.
Considere que a reação química genérica abaixo
ocorra com um rendimento de 100%.
3A(g) + 5Y(g) → W(g)
O volume do gás Y necessário para reagir com
1,5 mol do gás A a uma temperatura de 27ºC e
pressão de 16,4 atm é de:
Dado: R: 0,082 atm.L.mol-1.K-1
Qual o pH de uma solução de um ácido fraco,
monoprótico de concentração 2 mol/L.?
Dado: Ka = 1,8.10-5 a 25ºC, log 6 = 0,78
Assinale a alternativa que contém a geometria dos respectivos íons: carbonato, nitrito, sulfato, clorato e perclorato.
A reação química abaixo possui um ΔH= – 312
kJ/mol.
CH4(g) + 3 Cl2(g) → HCCl3(g) + 3HCl(g)
Dados: Energia de ligação (valores médios): C – H: 413
kJ/mol, H – Cl: 431 kJ/mol, C – Cl: 328 kJ/mol. A energia em módulo da ligação covalente na
molécula Cl2(g) é:
A combustão completa de 8,4g de um hidrocarboneto
produz 26,4g de CO2. A alternativa que
melhor representa a fórmula molecular desse
hidrocarboneto é:
Dados: C: 12 g/mol, H: 1 g/mol, O: 16 g/mol.
Considere a semi-reação abaixo no estado
padrão:
Após um procedimento químico a concentração
dos íons Pb2+
(aq) nesse equilíbrio era de 10-6 mol/L.
O potencial de redução da semi-reação acima
após o procedimento químico a 25ºC é de: Equação de Nerst a 25ºC:
Um determinado volume (V ) de um ácido forte monoprótico com pH = 2 foi diluido com água destilada até um volume de 20V. O valor do pH da solução diluída a 25ºC é de: Dado: log 5 = 0,7.
Assinale a alternativa que contém a solução aquosa com menor temperatura de congelação.