Marque a alternativa correta:
O sulfato é um dos íons mais abundantes na água marinha e estuarina, estando presente nas seguintes formas e proporções médias: SO42- (39%), Na2SO4 (37%), MgSO4 (19%) e CaSO4 (4%), a 250ºC e pH 8. Um método simples e acessível rotineiramente usado na determinação de sulfato em amostras de água baseia-se na adição de uma solução de cloreto de bário na amostra contendo o íon sulfato, conforme a seguinte reação:

Considere que a quantidade do reagente precipitante adicionado à amostra tem concentração estequiometricamente suficiente para reagir com a concentração de sulfato previamente estimada como normal para águas doces e marinhas, e que ocorre a formação de sulfato de bário em suspensão coloidal. Diante do exposto, assinale a alternativa que representa a técnica de análise que pode ser empregada para a determinação de sulfato, com base na medida da redução da transmissão de luz no meio causada pela formação de partículas.
Em análises quantitativas, um padrão primário, preparado por pesagem direta de uma substância suficientemente pura e diluição até determinado volume de solução é frequentemente empregado como solução de referência. Nesse contexto, assinale a alternativa correta.
Através de análise gravimétrica, o Ca++ em águas naturais pode ser determinado após adição de H2C2O4 e alcalinização com NH3, o que leva à formação do precipitado CaC2O4, que, após aquecimento a 1200°C, é convertido a CaO. Acerca disso, analise as proposições abaixo.
1) O produto da reação do Ca++ com H2C2O4 é um sal insolúvel que pode ser corretamente chamado de oxalato de cálcio.
2) O composto H2C2O4, adicionado na metodologia descrita, pode ser considerado um oxiácido forte, chamado corretamente de ácido oxálico.
3) A partir das condições descritas na metodologia, a base forte Ca(OH)2, chamada corretamente de hidróxido de cálcio, pode ser obtida.
Está(ão) correta(s), apenas:
A validação de métodos analíticos é fundamental nas análises químicas, para garantir que a metodologia desenvolvida seja adequada àquilo que se pretende. A respeito do teste de recuperação nas análises químicas de diferentes compostos em matrizes complexas, analise as proposições abaixo.
1) A recuperação permite avaliar a interferência dos componentes da matriz na separação, detecção e quantificação dos compostos de interesse.
2) A recuperação permite avaliar a eficiência do método de separação-purificação (ex. extração líquido-líquido) no pré-tratamento da matriz.
3) Valores de recuperação próximos a 100% indicam os melhores métodos de separação-purificação, pois permitem análises químicas com elevada precisão.
4) Mesmo métodos analíticos com baixos valores de recuperação (<5%) permitem determinar os compostos de interesse em matrizes complexas com adequada precisão, exatidão e linearidade.
Estão corretas, apenas:
Após as manipulações cotidianas em um laboratório de química, o técnico lavou a vidraria utilizada e a colocou na estufa para secagem. O técnico errou se colocou na estufa
Com relação às interferências que podem ocorrer em espectrometria de absorção atômica em chama ( F AAS ) e em espectrometria de absorção atômica em forno de grafite ( GF AAS ), qual a alternativa com as afirmações corretas?
I) As interferências químicas podem ocorrer devido à formação, durante o processo de atomização, de espécies moleculares do analito termicamente instáveis.
II) As interferências espectrais podem ser causadas devido a sinais de absorção de fundo gerados por espécies moleculares não completamente dissociadas e/ou devido à presença de material particulado sólido, suspenso no sistema de atomização.
III) Sinais de absorção de fundo podem ser corrigidos empregando-se um sistema instrumental de correção, baseado no uso de uma lâmpada de deutério, tanto para análises realizadas na região do ultravioleta, como também na região do visível do espectro eletromagnético.
IV) As determinações analíticas realizadas pela técnica de GF AAS são mais susceptíveis à ocorrência de interferências espectrais do que aquelas realizadas pela técnica de F AAS.
V) As determinações analíticas realizadas pela técnica de F AAS são mais susceptíveis à ocorrência de interferências espectrais do que aquelas realizadas pela técnica de GF AAS.
Sobre a química de coordenação e estruturas eletrônicas, assinale apenas a alternativa CORRETA.
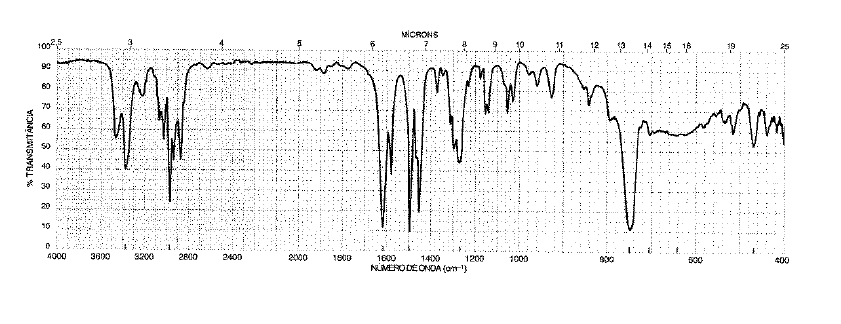
Determine a estrutura da substância desconhecida baseando-se no seu espectro infravermelho (IV) apresen-tado.
As medições químicas são realizadas em diversos ramos da atividade humana. Segundo o INMETRO, o objetivo principal da Metrologia Química é prover confiança para essas medições. Para alcançar esses objetivos são desenvolvidos materiais de referência, métodos, procedimentos e protocolos de referência, além de avaliação de laboratórios e capacitação de profissionais. Com relação aos conceitos relacionados com a Metrologia Química, assinale a alternativa CORRETA:
Com relação à espectrometria de absorção atômica em chama ( F AAS ), considerando a aplicação do procedimento de aspiração contínua (procedimento convencional) de solução de amostras, qual a alternativa com as afirmações incorretas?
I) Pode ser aplicada para a determinação de íons metálicos.
II) É uma técnica instrumental analítica mais sensível para a realização de determinações, em comparação à espectrometria de absorção atômica em forno de grafite ( GF AAS ).
III) Não permite a atomização do analito em um ambiente mais livre da presença de componentes da matriz da amostra.
IV) É uma técnica instrumental analítica fortemente afetada pelo efeito de interferências espectrais.
V) Possibilita a correção de sinais de absorção de fundo que ocorrem em comprimentos de onda da região do visível do espectro eletromagnético, mediante a utilização do sistema instrumental de correção com lâmpada de deutério.
As afirmações abaixo estão relacionadas à fonte de ionização por impacto de elétrons ( EI ) empregada na espectrometria de massas.
I) Aplicada a moléculas de média e de baixa polaridade em qualquer faixa de massa molecular.
II) Empregada na determinação da massa molecular dos compostos devido ao aparecimento do íon molecular em todos os espectros de massas.
III) Empregada na identificação de compostos devido ao grande número de fragmentos formados.
IV) Aplica-se a moléculas de média e de baixa polaridade em analitos com massa molecular inferior a 1.000 daltons.
Assinale a alternativa com as afirmações corretas.
A determinação da concentração total de Cálcio ( Ca ) por espectrometria de absorção atômica em chama ( F AAS ) pode ser realizada empregando-se a chama ar-acetileno ou a chama óxido nitroso-acetileno. Considerando que uma amostra de interesse para a determinação do referido elemento contenha fósforo (P ) na forma de fosfato ( PO 43- ), em concentração relativamente elevada em relação à concentração do analito, qual a alternativa com as afirmações corretas?
I) Recomenda-se a adição de concentração elevada de La3+ na forma de cloreto a todas as soluções envolvidas na análise, considerando-se a utilização da chama aracetileno como sistema de atomização.
II) Recomenda-se a adição de K+ ou Cs+ na forma de cloretos, a todas as soluções envolvidas na análise, considerando-se a utilização da chama óxido nitroso-acetileno como sistema de atomização.
III) A interferência de ionização pode ser eliminada utilizando-se a chama óxido nitrosoacetileno como sistema de atomização, ou adicionando-se um supressor (tampão) de ionização a todas as soluções envolvidas na análise.
IV) A interferência de ionização pode ser evitada empregando-se a chama ar-acetileno como sistema de atomização.
V) A determinação de Ca mediante o uso da chama ar-acetileno, independentemente de sua concentração em uma amostra, não exige a utilização de agente de liberação, até mesmo quando presente em uma matriz que contém uma concentração relativa muito elevada de P.
Atualmente existe uma diversidade de técnicas analíticas para a se determinar a composição química, mineralógica e microestrutural de compostos orgânicos e inorgânicos. Com relação aos métodos instrumentais de análise marque V para as afirmativas verdadeiras e F, para as falsas.
( ) Os espectros de absorção de radiação no ultravioleta e no visível são um instrumento que pode ser usado para a identificação de compostos orgânicos insaturados e também na elucidação de suas estruturas.
( ) A difração de Raio-X usa a lei de Bragg para calcular a distância entre camadas atômicas em um cristal. Esta técnica é de grande interesse para identificação dos elementos químicos presentes em uma amostra e para obtenção de estruturas moleculares e cristalinas.
( ) A espectroscopia de energia dispersiva pode ser utilizada para a determinação qualitativa e quantitativa da composição de amostras sólidas e líquidas, esta usa o princípio de identificação pelo raio-X emitido através da interação inelástica do feixe eletrônico com a amostra.
( ) A fluorescência de Raio-X é uma técnica não destrutiva que envolve o uso da emissão de RaioX para se obter uma análise elementar quantitativa de materiais no estado sólido e Hquido.
( ) A cromatografia gasosa pode ser usada para análises qualitativas e quantitativas. Na cromatografia gás-líquido a fase móvel é um gás, enquanto a fase estacionária é um líquido retido na superfície de um sólido inerte por adsorção ou ligação química.
Assinale a alternativa que contém a sequência CORRETA de cima para baixo.
Sobre o processo de atomização em espectrometria de absorção atômica em forno de grafite ( GF AAS ), qual a alternativa com a afirmação incorreta?