O consumo exagerado de refrigerantes é preocupante, pois contribui para o aumento de casos de obesidade e diabetes. Considere dois refrigerantes enlatados, um comum e um diet, e que ambos possuam a mesma quantidade de aditivos, exceto pela presença de açúcar. O refrigerante comum contém basicamente água carbonatada e grande quantidade de açúcar; já o refrigerante diet tem água carbonatada e adoçantes, cujas massas são muito pequenas.
CAVAGIS, A. D. M.; PEREIRA, E. A.; OLIVEIRA, L. C. Um método simples para avaliar o teor de sacarose e CO2
em refrigerantes. Química Nova na Escola, n. 3, ago. 2014 (adaptado)
Entre as duas versões apresentadas, o refrigerante comum possui
O soro fisiológico é uma solução aquosa de
cloreto de sódio (NaCl) comumente utilizada para
higienização ocular, nasal, de ferimentos e de lentes
de contato. Sua concentração é 0,90% em massa e
densidade igual a 1,00 g/mL.
Qual massa de NaCl, em grama, deverá ser adicionada à
água para preparar 500 mL desse soro?
A hidroponia pode ser definida como uma técnica
de produção de vegetais sem necessariamente a
presença de solo. Uma das formas de implementação
é manter as plantas com suas raízes suspensas em
meio líquido, de onde retiram os nutrientes essenciais.
Suponha que um produtor de rúcula hidropônica
precise ajustar a concentração do íon nitrato (NO3)
para 0,009 mol/L em um tanque de 5 000 litros e, para
tanto, tem em mãos uma solução comercial nutritiva
de nitrato de cálcio 90 g/L. As massas molares dos
elementos N, O e Ca são iguais a 14 g/mol, 16 g/mol e
40 g/mol, respectivamente.
Qual o valor mais próximo do volume da solução nutritiva,
em litros, que o produtor deve adicionar ao tanque?
A obtenção de sistemas coloidais estáveis depende
das interações entre as partículas dispersas e o meio
onde se encontram. Em um sistema coloidal aquoso,
cujas partículas são hidrofílicas, a adição de um solvente
orgânico miscível em água, como etanol, desestabiliza
o coloide, podendo ocorrer a agregação das partículas
preliminarmente dispersas.
A desestabilização provocada pelo etanol ocorre porque
A cafeína é um alcaloide, identificado como 1,3,7-trimetilxantina (massa molar igual a 194 g/mol), cuja estrutura química contém uma unidade de purina, conforme representado. Esse alcaloide é encontrado em grande quantidade nas sementes de café e nas folhas de chá-verde. Uma xícara de café contém, em média, 80 mg de cafeína.

Considerando que a xícara descrita contém um volume de 200 mL de café, a concentração, em mol/L, de cafeína nessa xícara é mais próxima de:
O vinagre vem sendo usado desde a Antiguidade
como conservante de alimentos, bem como agente de
limpeza e condimento. Um dos principais componentes
do vinagre é o ácido acético (massa molar 60 g/mol), cuja
faixa de concentração deve se situar entre 4% a 6% (m/v).
Em um teste de controle de qualidade foram analisadas
cinco marcas de diferentes vinagres, e as concentrações
de ácido acético, em mol/L, se encontram no quadro.

A amostra de vinagre que se encontra dentro do limite de
concentração tolerado é a
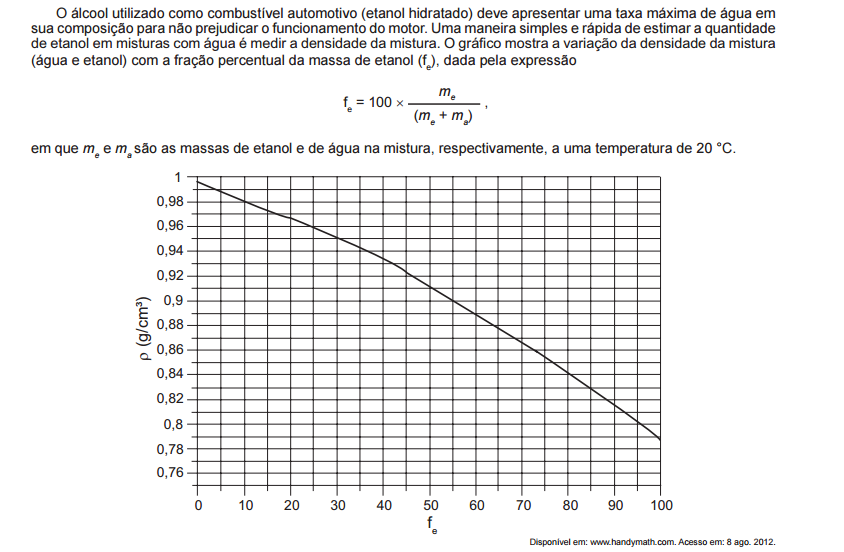
Suponha que, em uma inspeção de rotina realizada em determinado posto, tenha-se verificado que 50,0 cm3 de alcool
combustível tenham massa igual a 45,0 g. Qual é a fração percentual de etanol nessa mistura?
Em um caso de anemia, a quantidade de sulfato de ferro(II) (FeSO4, massa molar igual a 152 g/mol) recomendada como suplemento de ferro foi de 300 mg/dia. Acima desse valor, a mucosa intestinal atua como barreira, impedindo a absorção de ferro. Foram analisados cinco frascos de suplemento, contendo solução aquosa de FeSO4, cujos resultados encontram-se no quadro.

Se for ingerida uma colher (10 mL) por dia do medicamento para anemia, a amostra que conterá a concentração de sulfato de ferro(II) mais próxima da recomendada é a do frasco de número
O álcool comercial (solução de etanol) é vendido na concentração de 96%, em volume. Entretanto, para que possa ser utilizado como desinfetante, deve-se usar uma solução alcoólica na concentração de 70%, em volume. Suponha que um hospital recebeu como doação um lote de 1 000 litros de álcool comercial a 96%, em volume, e pretende trocá-lo por um lote de álcool desinfetante.
Para que a quantidade total de etanol seja a mesma nos dois lotes, o volume de álcool a 70% fornecido na troca deve ser mais próximo de
A utilização de processos de birremediação de resíduos gerados pela combustão incompleta de compostos orgânicos tem se tornado crescente, visando minimizar a poluição ambiental. Para ocorrência de resíduos de naftaleno, algumas legislações limitam sua concentração em até 30mg/Kg para solo agrícola e 0,14mg/L para água subterrânea. A quantificação desse resíduo foi realizada em diferentes ambientes, utilizando-se amostras de 500 g de solo e 100 mL de água, conforme apresentado no quadro.
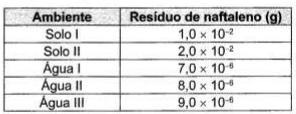
O ambiente que necessita de biorremediação é o(a)
O quadro apresenta o teor de cafeína em diferentes
bebidas comumente consumidas pela população.
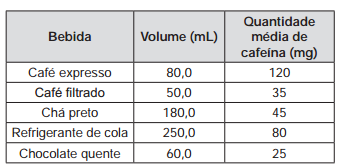
Da análise do quadro conclui–se que o menor teor de
cafeína por unidade de volume está presente no

Todos os organismos necessitam de água e grande parte deles vive em rios, lagos e oceanos. Os processos bio - lógicos, como respiração e fotossíntese, exercem profunda influência na química das águas naturais em todo o planeta. O oxigênio é ator dominante na química e na bioquímica da hidrosfera. Devido a sua baixa solubilidade em água (9,0 mg/l a 20ºC) a disponibilidade de oxigênio nos ecossistemas aquáticos estabelece o limite entre a vida aeróbica e anaeróbica. Nesse contexto, um parâmetro chamado Demanda Bioquímica de Oxigênio (DBO) foi definido para medir a quantidade de matéria orgânica presente em um sistema hídrico. A DBO corresponde à massa de O2 em miligramas necessária para realizar a oxidação total do carbono orgânico em um litro de água.
BAIRD, C. Química Ambiental. Ed. Bookman, 2005 (adaptado).
Dados: Massas molares em g/mol: C = 12; H = 1; O = 16.
Suponha que 10 mg de açúcar (fórmula mínima CH2O e massa molar igual a 30 g/mol) são dissolvidos em um litro de água; em quanto a DBO será aumentada?
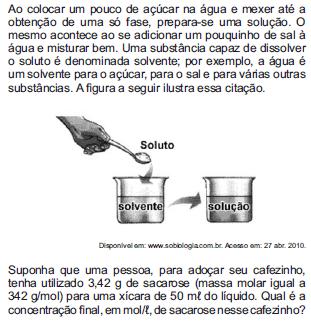
Os exageros do final de semana podem levar o indivíduo a um quadro de azia. A azia pode ser descrita como uma sensação de queimação no esôfago, provocada pelo desbalanceamento do pH estomacal (excesso de ácido clorídrico). Um dos antiácidos comumente empregados no combate à azia é o leite de magnésia.
O leite de magnésia possui 64,8 g de hidróxido de magnésio (Mg(OH)2) por litro da solução. Qual a quantidade de ácido neutralizado ao se ingerir 9 mL de leite de magnésia?
Dados: Massas molares (em g mol-1): Mg=24,3; C1=35,4; 0=16; H=1.

