Em dias muito frios, é comum que encanamentos de água se rompam devido ao processo de congelamento. Esse fenômeno é atribuído ao fato de a água se expandir ao congelar. Quanto trabalho, em joules, uma amostra de 100 g de água realiza ao congelar em 0 ºC e estourar um cano de água que exerce uma pressão oposta de 1,070 atm?
(As densidades da água e do gelo, em 0 °C, são 1,00 e 0,92 g cm-3, respectivamente. w = - Pext ∆V; 1 L atm = 101,325 J)
Uma máquina térmica reversível recebe calor de uma fonte quente (750 K) e rejeita calor em uma fonte fria (250 K) operando em ciclos. Se em cada ciclo o trabalho fornecido é 200 J, a energia fornecida pelo reservatório quente, em joules, em cada ciclo será

A figura precedente representa dois blocos A e B com massas iguais a 6 kg e 4 kg, respectivamente, inicialmente em repouso e ligados por um fio ideal (sobre uma roldana igualmente ideal). O coeficiente de atrito entre A e o plano horizontal vale 0,4 e a aceleração da gravidade vale 10 m/s 2.
Com base nas informações apresentadas e assumindo que toda a energia dissipada pela força de atrito foi usada para aquecer o corpo A, julgue o item a seguir.
Se o corpo A é feito de material que apresenta calor específico igual a 378 J/kgºC (Cobre), então, após ele ter sido arrastado por 1cm, sua temperatura terá aumentado em mais de 0,1 milésimos de Kelvins.
Sobre o processo de transferência de calor por radiação, analise as afirmativas abaixo:
I - A radiação emitida por um corpo negro é função do comprimento de onda, da temperatura e da direção.
II - Na distribuição de Planck a radiação emitida varia continuamente com o comprimento de onda.
III - Pela distribuição de Planck a radiação de corpo negro depende unicamente da temperatura.
Está CORRETO apenas o que se afirma em:
A variação do volume de bolhas de ar em um meio líquido como o sangue depende da pressão do meio externo sobre as paredes da bolha e está associada a problemas graves de saúde como a embolia pulmonar gasosa, e consiste de um problema muito estudado na literatura médica, biológica e biofísica.
Considere que pequenas bolhas de gás ideal são formadas no fundo de um recipiente com uma coluna de água de 20cm. Ao se desprenderem do fundo irão pela ação do empuxo serem trazidas à superfície que está à pressão de 1atm = 105 Pa. Considere a densidade da água de 1000 kg/m3 e g = 10m/s2 . A temperatura do fluido ao longo do recipiente é constante. O aumento percentual no volume da bolha será de:
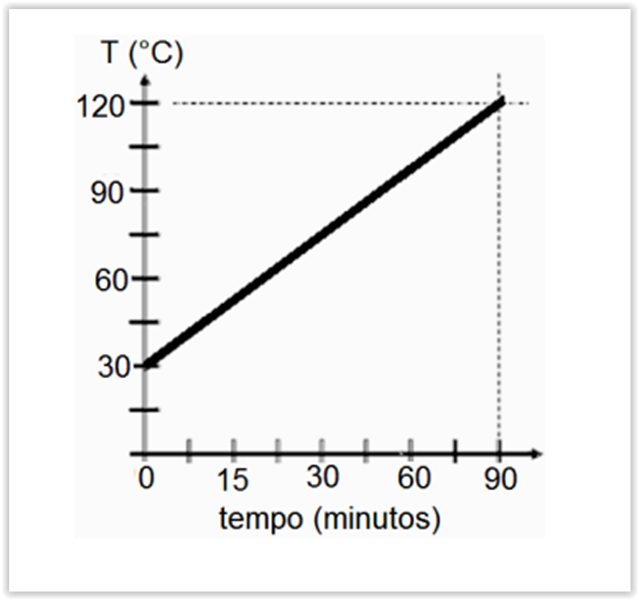
Três quartos de quilograma de uma substância desconhecida são aquecidos à taxa de 75 calorias por minuto, e a
variação de temperatura foi acompanhada conforme apresentado no gráfico abaixo. Com base nessas informações, o
calor específico da referida substância, em cal g-1 K-1
, é igual a:
Um gás ideal inicialmente a 0,85 atm e 66 ºC, expande-se até que seu volume, pressão e temperatura sejam respectivamente 94 mL, 0,60 atm e 45 °C. Sob tais condições, o volume inicial desse gás era de, aproximadamente:
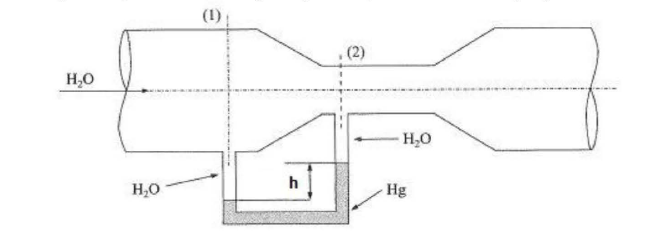
Nas indústrias químicas existe uma diversidade de processos que envolvem fluidos. Uma das variáveis de controle nesse caso é a vazão do fluido que escoa por certa tubulação horizontal. Para isso, pode-se usar um tubo Venturi para medir tal vazão. Assinale a alternativa CORRETA que contenha a expressão do cálculo da vazão de acordo com as respectivas variáveis do processo para um tubo circular. Considere a área da seção transversal (1) duas vezes maior que da seção (2), regime turbulento e despreze perdas de carga. Admita que: Q 1 é a vazão na seção (1); D1 é o diâmetro do tubo na seção (1); g é a aceleração da gravidade; h é a diferença de altura apontada no Venturi; p.H9 e p.H20 são as massas específicas do mercúrio e da água, respectivamente; e y é o peso específico do fluido que passa no tubo (1).
A primeira lei da termodinâmica pode ser considerada como outra forma de enunciar a lei da conservação da energia, ou seja, a variação de energia de um sistema é igual à diferença entre a energia recebida pelo sistema e a energia fornecida por um sistema. A respeito da primeira lei da termodinâmica, julgue o próximo item.
Um gás é aquecido e descreve uma reta vertical em um
diagrama PV do estado inicial (2,0 · 10 5 Pa e 4 m³ ) ao
estado final (5,0 · 105 Pa e 3 m³ ). O trabalho realizado
pelo gás sobre o ambiente é de 900 kJ.
Sobre equilíbrio químico, considere as afirmativas a seguir e assinale a alternativa correta:
I. As reações não vão até o fim. Elas continuam até que a composição da mistura reacional corresponda ao mínimo de entalpia. Essa composição é descrita por uma constante de equilíbrio característica da reação que depende da temperatura, dentre outros fatores.
II. Para controlar o rendimento de uma reação, precisamos entender a base termodinâmica do equilíbrio e como a posição atual de equilíbrio é afetada por condições como a temperatura e a pressão, por exemplo.
III. O equilíbrio químico é o estágio da reação química em que não existe mais tendência a mudar a composição da mistura da reação, isto é, as concentrações ou pressões parciais dos reagentes e produtos. Como os equilíbrios físicos, todos os equilíbrios químicos são dinâmicos, com a reação direta e inversa ocorrendo com a mesma velocidade.
IV. A termodinâmica descreve quantitativamente o equilíbrio, o que nos possibilita controlar a direção e o rendimento das reações.
V. A composição de uma mistura de reação no equilíbrio é descrita pela constante de equilíbrio, que é dependente do produto das atividades dos produtos (elevadas a potências iguais aos coeficientes estequiométricos da equação química balanceada da reação) dividido pelo produto das atividades dos reagentes (elevadas a potências iguais a seus coeficientes estequiométricos).
Assinale a alternativa correta:
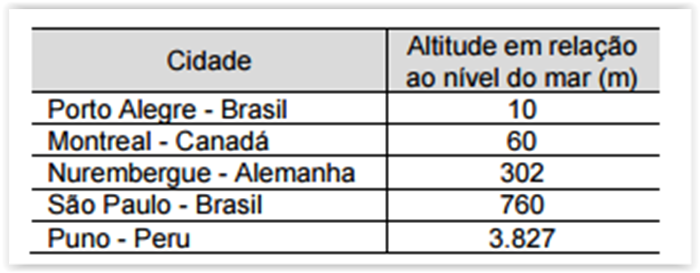
Considerar as localidades abaixo e suas respectivas
altitudes em relação ao nível do mar:
A menor temperatura de ebulição da água é observada
em:
A figura a seguir ilustra um diagrama T–S (temperatura (T )
versus entropia (S )) de um motor que obedece a um ciclo de Carnot
ideal, tendo como substância de trabalho um gás ideal.

Considerando que o trabalho realizado por esse sistema seja igual
a 3.000 J, julgue os próximos itens.
Em um ciclo completo, a variação de energia interna é igual
a 3.000 J.
A figura a seguir ilustra um diagrama T–S (temperatura (T )
versus entropia (S )) de um motor que obedece a um ciclo de Carnot
ideal, tendo como substância de trabalho um gás ideal.

Considerando que o trabalho realizado por esse sistema seja igual
a 3.000 J, julgue os próximos itens.
A diferença entre as energias absorvida e transferida pelo
sistema é de 1.500 J.
A figura a seguir ilustra um diagrama T–S (temperatura (T )
versus entropia (S )) de um motor que obedece a um ciclo de Carnot
ideal, tendo como substância de trabalho um gás ideal.

Considerando que o trabalho realizado por esse sistema seja igual
a 3.000 J, julgue os próximos itens.
O trabalho realizado pelo gás entre os estados B e C é igual a
três quartos da energia interna no ponto B.
No estudo de Termoquímica, o professor propôs uma experiência
para determinação do calor de combustão do álcool etílico
(etanol).
O procedimento experimental e as anotações de um grupo de
alunos estão apresentados a seguir:
I. preparar a lamparina colocando uma quantidade suficiente
de álcool etílico para que a combustão possa ser realizada.
II. determinar a massa do sistema “álcool-lamparina” (mi) e
anotar no caderno. Valor anotado mi= 180,0 g;
III. determinar a massa do erlenmeyer (me) vazio e anotar no
caderno. Valor anotado me = 200,0 g;
IV. medir 100 mL de água, que correspondem a 100 g, em uma
proveta e transferir para o erlenmeyer. Envolver as paredes
do erlenmeyer com jornal e prender com fita crepe. Colocar
em um suporte;
V. medir a temperatura da água (Ti) e anotar o valor.
Valor anotado Ti = 25°C;
VI. acender a lamparina e aquecer a água do erlenmeyer,
durante 5 minutos. Após esse tempo, apagar a lamparina e
medir a temperatura da água (Tf) e anotar o valor. Valor
anotado Tf = 40°C;
VII. Medir, após algum tempo, a massa do sistema
“álcool-lamparina”(mf) após a combustão. Valor anotado
mf = 160,0 g.
Utilizando os dados anotados e a constante 1,0 cal.g–1.°C–1 como
calor específico da água e a constante 0,2 cal.g–1.°C–1 como calor
específico do vidro, os alunos devem chegar a um valor para o
calor de combustão do álcool, em cal.g–1, de