Na escala de temperatura Fahrenheit, o ponto de fusão da água corresponde a 32 °F, enquanto o ponto de ebulição da água corresponde a 212 °F. Na escala de temperatura Celsius, esses pontos correspondem, respectivamente, a 0 °C e 100 °C.
A tabela a seguir apresenta os estados do corpo humano correspondentes a diferentes temperaturas.
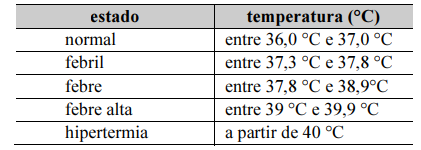
Com base no texto e na tabela precedentes, assinale a opção correta.
A tabela a seguir informa o calor específico de algumas substâncias.

I. A água, por ter um calor específico muito alto, é um excelente elemento termorregulador. A ausência de água faz com que, nos desertos, ocorram enormes diferenças entre a temperatura máxima e a mínima em um mesmo dia.
II. Para refrigerar uma peça aquecida, é comum mergulhá-la em água. Será mais eficiente, para resfriá-la, mergulhá-la em mercúrio. Só não se faz isso porque, além de muito caro, seus vapores são extremamente tóxicos.
III. Se cedermos a mesma quantidade de calor a amostras de massas iguais de alumínio e ferro, a temperatura da amostra de ferro aumentará o dobro do que aumenta a amostra de alumínio.
Está correto o que se afirma em
Duas amostras “A” e “B” de água no estado líquido de mesma massa (m) e mesmo calor específico (c) possuem temperatura iniciais diferentes TIA e TIB, sendo TIA maior que TIB. A mistura obtida com as duas amostras, após algum tempo, atinge a temperatura final TF. A quantidade de calor que a amostra “A” cedeu é igual a ____.
Mesmo para peixes de aquário, como o peixe arco-íris, a temperatura da água fora da faixa ideal (26 °C a 28 °C), bem como sua variação brusca, pode afetar a saúde do animal. Para manter a temperatura da água dentro do aquário na média desejada, utilizamse
dispositivos de aquecimento com termostato. Por exemplo, para um aquário de 50 L, pode-se utilizar um sistema de aquecimento de 50 W otimizado para suprir sua taxa de resfriamento. Essa taxa pode ser considerada praticamente constante, já que a temperatura externa ao
aquário é mantida pelas estufas. Utilize para a água o calor específico 4,0 kJ kg−1 K−1 e a densidade 1 kg L−1.
Se o sistema de aquecimento for desligado por 1 h, qual o valor mais próximo para a redução da temperatura da água do aquário?
A composição de um dos refrigerantes mais ácidos mundialmente consumido é mantidaem segredo pelos seus produtores. Existe uma grande especulação em torno da "fórmula"dessa bebida, a qual envolve algumas das seguintes substâncias:
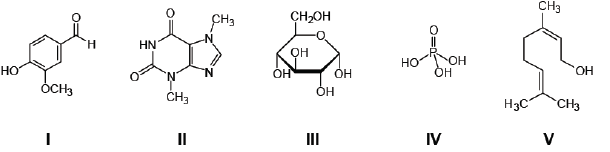
A substância presente nesse refrigerante, responsável pelo seu acentuado caráter ácido, é a
Na cidade de São Paulo, as ilhas de calor são responsáveis pela alteração da direção do fluxo da brisa marítima que deveria atingir a região de mananciais. Mas, ao cruzar a ilha de calor, a brisa marítima agora encontra um fluxo de ar vertical, que transfere para ela energia térmica absorvida das superfícies quentes da cidade, deslocando-a para altas altitudes. Dessa maneira, há condensação e chuvas fortes no centro da cidade, em vez de na região de mananciais. A imagem apresenta os três subsistemas que trocam energia nesse fenômeno.
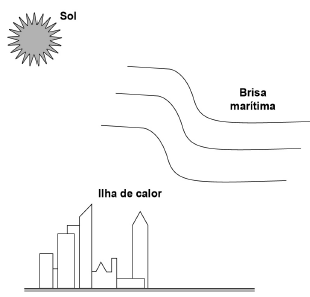
No processo de fortes chuvas no centro da cidade de São Paulo, há dois mecanismos dominantes de transferência de calor: entre o Sol e a ilha de calor, e entre a ilha de calor e a brisa marítima.
VIVEIROS, M. Ilhas de calor afastam chuvas de represas. Disponível em: www2.feis.unesp.br.
Acesso em: 3 dez. 2019 (adaptado).
Esses mecanismos são, respectivamente,
Na maioria das vezes, a água pode ser utilizada para evitar incêndios. Entretanto, nem todos os tipos de incêndio podem ser apagados com água.
Uma propriedade física importante da água e que contribui para a utilização dela como meio para se evitar incêndios é a(o)
Um ebulidor é um aparelho que funciona por efeito joule. Quando ligado em 110V e colocado dentro de um béquer contendo 0,5 kg de água a uma temperatura de 20°C, consegue elevar a temperatura dessa amostra para 80°C em 4,0 minutos.

Dados:
• calor específico da água c = 4,0J/g°C
• 1 cal = 4,0 J
Considerando que toda a energia liberada pelo ebulidor seja utilizada para aquecer apenas a água, podemos afirmar que a potência dele vale
Uma quantidade de gelo é aquecida do ponto de fusão (TF) até uma temperatura acima do ponto de ebulição da água (TE). O gráfico que melhor expressa a entropia S em função da temperatura T nesse processo é
Um mole de um gás monoatômico ideal, inicialmente a uma temperatura T, se expande de um volume V até um volume 2V em duas situações:
(i) a temperatura constante;
(ii) a pressão constante.
Com relação ao trabalho realizado na expansão e ao calor absorvido pelo gás, em cada situação, é CORRETO afirmar que:
Dois objetos feitos do mesmo material (mármore, por exemplo) possuem capacidades térmicas proporcionais a suas massas. Assim, é conveniente definir uma “capacidade térmica por unidade de massa", ou calor específico (c), que se refere não a um objeto, mas a uma massa unitária do material de que é feito o objeto. Já quando o calor é transferido para uma amostra sólida ou líquida, nem sempre a temperatura da amostra aumenta. Em vez disso, a amostra pode mudar de fase (ou de estado). No caso, a quantidade de energia por unidade de massa que deve ser transferida em forma de calor para que uma amostra mude totalmente de fase é chamada de calor de transformação e é representada pela letra L.
Halliday e Resnick. Fundamentos de Física: gravitação, ondas
e termodinâmica. v. 2. Rio de Janeiro: LTC, 2009 (com adaptações).
A partir do texto acima, assinale a alternativa que apresenta
a quantidade de calor que uma amostra de gelo de massa m = 100 g a –10 ºC deve absorver para passar ao estado líquido a 20 ºC, sendo o calor específico do gelo (cgelo) igual a 2.220 J/kg.K, o calor específico da água (cágua) igual a 4.190 J/kg.K e o calor de fusão do gelo (LF) igual a 333 kJ/kg.
Dentro de um calorímetro de capacidade térmica desprezível, são misturados 200 g de esferas de ferro à temperatura de 100°C e 500 g de água à temperatura de 20°C. O sistema é fechado e, após um determinado tempo, podemos afirmar que a temperatura de equilíbrio vale, aproximadamente:
Dados: Calor específico da água: 1 cal/g°C; calor específico do ferro: 0,11 cal/g°C.
Em um experimento, é fornecido calor a uma substância, inicialmente no estado sólido, que promove seu aquecimento e mudança de estado físico. O calor de vaporização da substância vale 200 cal.g -1. O gráfico do calor recebido em função da temperatura da substância é mostrado na Figura abaixo.

O calor específico dessa substância no estado líquido, em cal.g-1.°C-1, é, aproximadamente,
Um bloco plano de espessura ΔL0 é composto por um material homogêneo e isotrópico. Se a diferença de temperatura entre duas superfícies paralelas do bloco é ΔT0, tem-se um fluxo de calor entre essas superfícies dado por Q'0.
Se o material que forma o bloco for substituído por outro com as mesmas dimensões, mas com apenas 40% de sua condutividade térmica, ao observar-se o mesmo fluxo de calor, a nova diferença de temperatura entre as superfícies do bloco será
Uma lâmpada incandescente consiste de um filamento no vácuo. Em condições normais de funcionamento o filamento tem uma temperatura de 1600 K. Outra lâmpada com um filamento similar, que está em um bulbo preenchido com gás, tem o filamento com temperatura de 3200 K. Considere que ambos os filamentos, neste processo, se comportam como corpos negros. Analisando-se os espectros das radiações emitidas pelo filamento no vácuo e pelo filamento no ar, respectivamente, verifica-se que a razão entre os comprimentos de onda nos quais as intensidades das radiações são máximas é de

