Em uma indústria alimentícia, para produção de doce de leite, utiliza-se um tacho de parede oca com uma entrada para vapor de água a 120 °C e uma saída para água líquida em equilíbrio com o vapor a 100 °C. Ao passar pela parte oca do tacho, o vapor de água transforma-se em líquido, liberando energia. A parede transfere essa energia para o interior do tacho, resultando na evaporação de água e consequente concentração do produto.
No processo de concentração do produto, é utilizada energia proveniente
A primeira lei da termodinâmica, associada ao conceito de energia, pode ser expressa pela diferença entre o calor absorvido e o trabalho realizado nos processos termodinâmicos.
Um gás ideal no estado inicial está com pressão de 3 atm, volume de 1 L e energia interna de 456 J, após sofrer dois processos sucessivos: um isobárico, até atingir o volume de
3 L, e outro isocórico, até atingir o estado final com pressão de 2 atm, volume de 3 L e energia interna de 912 J.
Considerando que 1 atm . L = 100,0 J, assinale a alternativa que indica qual o calor trocado durante o processo, em Joules (J).
O primeiro princípio da Termodinâmica estabelece que, se um sistema gasoso recebe uma quantidade de calor (Q) do meio externo, essa energia pode ser armazenada no sistema, aumentando sua energia interna ( U), e/ou pode ser utilizada na realização de trabalho (W).
Com base nesse princípio, em uma transformaçã
Na montagem de uma cozinha para um restaurante, a escolha do material correto para as panelas é importante, pois a panela que conduz mais calor é capaz de cozinhar os alimentos mais rapidamente e, com isso, há economia de gás. A taxa de condução do calor depende da condutividade k do material, de sua área A, da diferença de temperatura ΔT e da espessura d do material, sendo dada pela relação . Em panelas com dois materiais, a taxa de condução é dada por
, em que d1 e d2 são as espessuras dos dois materiais, e k e k são as condutividades de cada material. Os materiais mais comuns no mercado para panelas são o alumínio (k = 20 W/m K), o ferro (k = 8 W/m K) e o aço (k = 5 W/m K) combinado com o cobre (k = 40 W/m K).
Compara-se uma panela de ferro, uma de alumínio e uma composta de da espessura em cobre e da espessura em aço, todas com a mesma espessura total e com a mesma área de fundo.
A ordem crescente da mais econômica para a menos econômica é
As panelas de pressão reduzem o tempo de cozimento dos alimentos por elevar a temperatura de ebulição da água. Os usuários conhecedores do utensílio normalmente abaixam a intensidade do fogo em panelas de pressão após estas iniciarem a saída dos vapores.
Ao abaixar o fogo, reduz-se a chama, pois assim evita-se o(a
Na cidade de São Paulo, as ilhas de calor são responsáveis pela alteração da direção do fluxo da brisa marítima que deveria atingir a região de mananciais. Mas, ao cruzar a ilha de calor, a brisa marítima agora encontra um fluxo de ar vertical, que transfere para ela energia térmica absorvida das superfícies quentes da cidade, deslocando-a para altas altitudes. Dessa maneira, há condensação e chuvas fortes no centro da cidade, em vez de na região de mananciais. A imagem apresenta os três subsistemas que trocam energia nesse fenômeno.
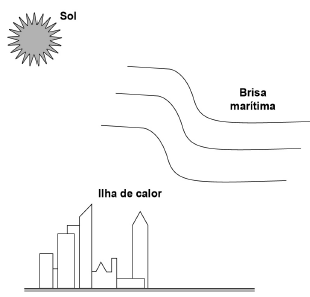
No processo de fortes chuvas no centro da cidade de São Paulo, há dois mecanismos dominantes de transferência de calor: entre o Sol e a ilha de calor, e entre a ilha de calor e a brisa marítima.
VIVEIROS, M. Ilhas de calor afastam chuvas de represas. Disponível em: www2.feis.unesp.br.
Acesso em: 3 dez. 2019 (adaptado).
Esses mecanismos são, respectivamente,
Tanto a conservação de materiais biológicos como o resfriamento de certos fotodetectores exigem baixas temperaturas que não são facilmente atingidas por refrigeradores. Uma prática comum para atingi-las é o uso de nitrogênio líquido, obtido pela expansão
adiabática do gás N2, contido em um recipiente acoplado a um êmbolo, que resulta no resfriamento em temperaturas que chegam até seu ponto de liquefação em −196 °C. A figura exibe o esboço de curvas de pressão em função do volume ocupado por uma quantidade de gás para os processos isotérmico e adiabático. As diferenças entre esses processos podem ser identificadas com base na primeira lei da
termodinâmica, que associa a variação de energia interna à diferença entre o calor trocado com o meio exterior e o trabalho realizado no processo.
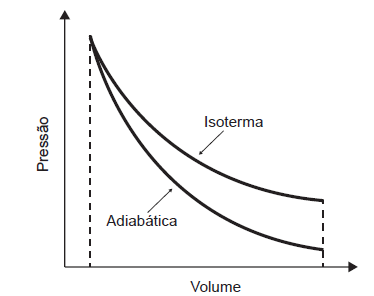
A expansão adiabática viabiliza o resfriamento do N2 porque
Sobre a lei da conservação de energia da termodinâmica, é correto afirmar que
É comum, na Termodinâmica, utilizar a seguinte expressão: (P1V1)/T1 é igual a (P2V2)/T2.Nessaexpressão, P, V e T representam, respectivamente, a pressão, o volume e a temperatura de uma amostra de um gás ideal. Os números representam os estados inicial (1) e final (2). Para utilizar corretamente essa expressão é necessário que o número de mols, ou de partículas, do estado final seja _________ do estado inicial e que a composição dessa amostra seja _________ nos estados final e inicial.
Assinale a alternativa que completa corretamente as lacunas da frase acima.
Um cilindro com um pistão móvel contém 1 kg de gás nitrogênio a pressão de 1 atm. Em um processo isobárico, uma quantidade de calor igual a 25 kcal é adicionada ao gás e sua energia interna aumenta de 8 kcal. A variação de volume do gás nesse processo é de, aproximadamente,

Um recipiente adiabático de volume V é dividido em dois volumes iguais V1 e V2. Inicialmente, um gás ideal é confinado no volume V1. O volume V2 é evacuado. A partição que separa os dois volumes é então removida e o gás que estava no volume V1 passa a ocupar os dois volumes V=V1 + V2. Se a temperatura inicial do gás era T0, podemos afirmar que
Em um determinado reservatório térmico, 500 g de água a 100 ºC são convertidos em vapor a 100 ºC, à pressão atmosférica de 1 atm. O volume da água varia de um valor inicial de 1 . 10‐3 m3 do líquido para 1,5 m3 do vapor, 1 atm ≅ 1 . 105 Pa e o calor latente de vaporização da água é igual a 2.256 kJ/kg.
Com base nessa situação hipotética, assinale a alternativa que apresenta o intervalo de variação da energia interna ( ΔEint) , em kJ, do sistema durante todo o processo.
Em relação a primeira lei da termodinâmica, qual alternativa abaixo é INCORRETA?
A primeira lei da termodinâmica pode ser considerada como outra forma de enunciar a lei da conservação da energia, ou seja, a variação de energia de um sistema é igual à diferença entre a energia recebida pelo sistema e a energia fornecida por um sistema. A respeito da primeira lei da termodinâmica, julgue o próximo item.
Um gás é aquecido e descreve uma reta vertical em um
diagrama PV do estado inicial (2,0 · 10 5 Pa e 4 m³ ) ao
estado final (5,0 · 105 Pa e 3 m³ ). O trabalho realizado
pelo gás sobre o ambiente é de 900 kJ.
A figura a seguir ilustra um diagrama T–S (temperatura (T )
versus entropia (S )) de um motor que obedece a um ciclo de Carnot
ideal, tendo como substância de trabalho um gás ideal.

Considerando que o trabalho realizado por esse sistema seja igual
a 3.000 J, julgue os próximos itens.
Em um ciclo completo, a variação de energia interna é igual
a 3.000 J.

