Para um procedimento de neutralização ácido-base, foi solicitada a adição de um determinado volume de uma solução de hidróxido de sódio 0,5 mol.L-1 em uma solução de ácido acético 1 mol.L-1. Entretanto, para esse procedimento, o laboratório dispõe apenas de uma solução estoque de hidróxido de sódio 2 mol.L-1. Nesse contexto, assinale a alternativa que apresenta o volume de solução de hidróxido de sódio 2 mol.L-1mL necessário para preparar 50 mL da solução de hidróxido de sódio 0,5 mol.L-1.
A água boricada é uma solução não estéril que contém água e ácido bórico (H3BO3) e é comercializada em drogarias, normalmente, nas concentrações de 2% e 3%. Qual a massa de ácido bórico 3% em uma embalagem de 250 mL?
Aldeídos e cetonas são classes de compostos orgânicos com algumas características comuns. A respeito desses compostos, assinale a alternativa correta.
Nos dias atuais, várias instrumentações analíticas permitem detecção e/ou quantificação de diferentes sustâncias químicas, mesmo em pequenas concentrações. Portanto, a adequada eliminação dos resíduos nos materiais, equipamentos e instrumentos de laboratório é uma etapa crucial para a análise. A esse respeito, assinale a alternativa correta.
A oxidação do ferro para a formação de ferrugem envolve várias etapas, mas pode ser descrita, de maneira simplificada, da seguinte forma:
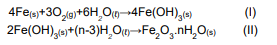
A esse respeito, assinale a alternativa correta.
Questão anterior:

De acordo com a metodologia descrita anteriormente para a determinação gravimétrica do cálcio (questão 37), a partir de 150 mL de uma amostra de água natural foram determinados 0,2941 g de CaO (56,077 g.moL-1). Qual a concentração de Ca (40,078 g.moL-1) na amostra de água, expressa em unidades de gramas por 100 mL de água?
O ácido benzoico (C 6H5COOH) é usado na produção do benzoato de sódio, um dos conservantes mais empregados na indústria dos alimentos, devido a sua propriedade antimicrobiana. Assinale a alternativa que apresenta o valor aproximado do pH de um solução de 0,1 mol.L-1 C6H5COOH, supondo que o grau de ionização (α) desse ácido é igual a 6,4x10-5.
(Dados: log 6,4=0,81)
Ainda com relação aos indicadores de padrão nacional de qualidade do ar, considere que em uma amostra de 1000 cm3 de ar atmosférico foram encontrados 5 nmols de dióxido de nitrogênio (NO2). Sabendo que o Conselho Nacional de Meio Ambiente (Conama) considera 320 µg.m3 níveis máximos aceitáveis (padrão primário) e 190 µg.m3 níveis desejáveis (padrão secundário) (Resolução CONAMA nº 03, de 28/06/90), assinale a alternativa que apresenta a concentração de NO2 e sua relação com os padrões de qualidade do ar estabelecidos.
(Dados: massa atômica N=14, O=16)
Questão anterior:

Ainda a respeito do método de Mohr empregado para determinação do Cl- em água do mar e as reações envolvidas nessa metodologia (descritas na questão 54), analise as informações descritas na tabela apresentada e assinale a alternativa correta.
Considere uma solução acidificada de nitrato de prata (AgNO3) como solução padrão e cromato de potássio (CrO4-2) como indicador.

A solução fisiológica constitui-se de 9,0 gramas de cloreto de sódio (NaCl) em um litro de água. Assinale a alternativa que apresenta a massa de NaCl em uma embalagem de 100 mL de soro fisiológico, expressa em percentagem.
Questão anterior:
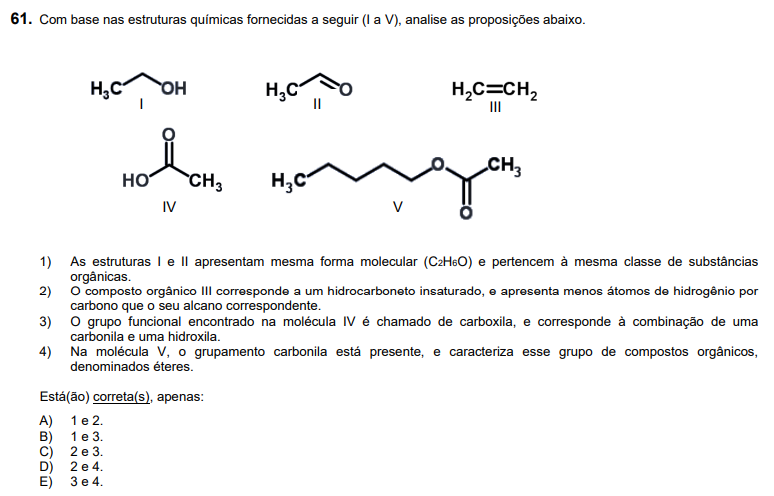
Ainda com base nos compostos orgânicos (I a V) apresentados na questão 61, com relação às diferentes reações orgânicas, assinale a alternativa correta.
Correlacione as ilustrações de vidrarias básicas comumente usadas em laboratórios de química com as informações a seguir.
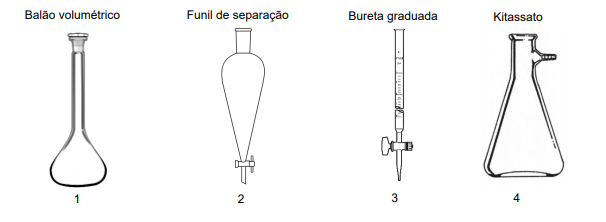
( ) Vidraria usada junto com o funil de Büchner em filtrações a vácuo.
( ) Vidraria de elevada precisão e exatidão analítica usada no preparo de soluções.
( ) Vidraria usada para separar líquidos imiscíveis de diferentes densidades.
( ) Vidraria usada na titulação de soluções.
A sequência correta, de cima para baixo, é:
A extração líquido-líquido baseia-se na diferença de solubilidade de um soluto em dois líquidos imiscíveis. Portanto, a quantidade do soluto que é extraída depende do seu coeficiente de partição ou coeficiente de distribuição (K) entre as duas fases líquidas. Qual a porcentagem aproximada de um soluto extraído para 100 mL de éter de petróleo, supondo que foram usados 100 mL de fase aquosa contendo 5 g do soluto, após agitação em funil de separação?

Através de análise gravimétrica, o Ca++ em águas naturais pode ser determinado após adição de H2C2O4 e alcalinização com NH3, o que leva à formação do precipitado CaC2O4, que, após aquecimento a 1200°C, é convertido a CaO. Acerca disso, analise as proposições abaixo.
1) O produto da reação do Ca++ com H2C2O4 é um sal insolúvel que pode ser corretamente chamado de oxalato de cálcio.
2) O composto H2C2O4, adicionado na metodologia descrita, pode ser considerado um oxiácido forte, chamado corretamente de ácido oxálico.
3) A partir das condições descritas na metodologia, a base forte Ca(OH)2, chamada corretamente de hidróxido de cálcio, pode ser obtida.
Está(ão) correta(s), apenas:
A respeito dos conhecimentos básicos necessários para a correta preparação e aplicação de soluções tampão, assinale V para as afirmações verdadeiras, ou F para as falsas.
( ) Solução tampão é uma mistura de um ácido fraco e sua base conjugada, ou uma base fraca e seu ácido conjugado.
( ) A diluição de uma solução tampão ou a adição de pequenas quantidades de ácidos ou bases provoca uma grande variação no pH final dessa solução.
( ) Para a manutenção do pH adequado em um experimento de digestão alcalina, a tripsina, que apresenta pH ótimo em torno de 8, deve ser incubada, preferencialmente, em solução tampão pH 6 ao invés de pH 9.
( ) Uma solução tampão pode ser preparada pela combinação de quantidades calculadas de um par ácido-base conjugado adequado.
A sequência correta, de cima para baixo, é:

