Amostras são frações de materiais de interesse analítico. A depender do problema a ser solucionado, procede-se à escolha da metodologia de análise para, então, definir a amostragem. É exemplo de tratamento químico preliminar, no preparo de amostra, o/a
O ponto final de uma titulação de 5mL de uma solução de NaOH com HCl (0,2 mol.L-1 ) foi observado quando foram adicionados 20mL de HCl. Assinale a alternativa que indica corretamente a concentração obtida durante a titulação da solução de NaOH.
O ácido oxálico (H2C2O4) está presente em caules e folhas de vegetais como o espinafre e a beterraba. Uma maneira de quantificar a concentração de ácido oxálico nos vegetais é através da titulação com hidróxido de sódio (NaOH). Para realizar uma titulação, pretende-se escolher um indicador adequado para o ponto de equivalência mostrado no gráfico. O quadro apresenta os indicadores disponíveis no laboratório.

O indicador adequado para essa titulação é o(a)
Dentre os solutos dissolvidos na água do mar, aqueles que estão presentes em maior quantidade são chamados de elementos conservativos, e correspondem a sais com proporção relativa constante entre si, que determinam a salinidade do mar. A esse respeito, assinale a alternativa correta.
Sobre Hidrólise, podemos afirmar, exceto:
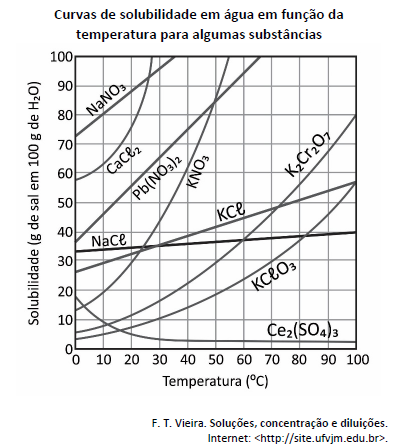
Deseja‐se preparar duas soluções saturadas na temperatura de 20 ºC, uma contendo o sal menos solúvel e outra contendo o sal mais solúvel nessa temperatura. Para cada uma das soluções, será empregado o mínimo possível dos sais e será utilizado 1 L de água, mantida a 20 ºC durante todo o processo de dissolução. A massa específica da água é igual a 1.000 kg m−3. Com base nesse caso hipotético e no gráfico, assinale a alternativa que apresenta, correta e respectivamente, as massas aproximadas dos dois sais necessárias para o preparo dessas soluções.
Questão anterior:

Ainda a respeito do método de Mohr empregado para determinação do Cl- em água do mar e as reações envolvidas nessa metodologia (descritas na questão 54), analise as informações descritas na tabela apresentada e assinale a alternativa correta.
Considere uma solução acidificada de nitrato de prata (AgNO3) como solução padrão e cromato de potássio (CrO4-2) como indicador.

Considerando que a solubilidade do acetato de sódio é igual a 123,5g / 100g de água a 20°C, no que se refere à dissolução do soluto, é correto afirmar que
A acidez titulável do leite é expressa em porcentagem (massa/volume) de ácido lático (menor ∝ - hidroxi-ácido carboxílico com isomeria óptica). Uma alíquota de 0,01 L de amostra de leite foi colocada em um erlenmeyer e adicionou-se 2 gotas de fenolftaleína. A titulação da amostra consumiu 1,68 cm3 de solução de NaOH 4,0 g.L-1.
A acidez do leite na amostra, expressa em porcentagem (massa/volume) é, aproximadamente:
A 25 ºC, o pH da água pura e de soluções aquosas neutras é igual a 7. Assinale a única alternativa que contém um composto cuja solução aquosa tem pH menor que 7, a 25 ºC.
Uma amostra de 2,00 mL de uma solução de Fe2+ de concentração desconhecida foram adicionados a 1,00 mL de água destilada, 2,00 mL de solução diluída de H2O2 e 1,00 mL de alcalina de luminol. A medida da quimiluminescência desta amostra indicou um sinal integrado de 16,1. Quando, a uma outra alíquota de 2,00 mL desta amostra, foi adicionado 1,00 mL de solução de Fe2+ a 4,75.10-5 mol/L, e os mesmos volumes das soluções de H2O2 e luminol, o sinal integrado de quimiluminescência foi 29,6. Considerando que a intensidade da quimiluminescência aumenta linearmente com a concentração de Fe2+, determine a concentração deste íon na amostra inicial e indique a alternativa que apresenta o valor correto.
Atenção: Para responder à questão, considere a curva de titulação abaixo.
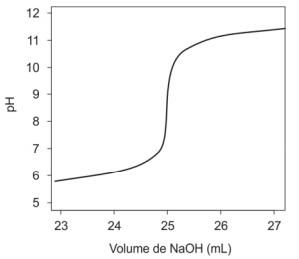
O gráfico representa a titulação de