Abaixo estão representados cinco frascos contendo soluções aquosas diluídas dos compostos indicados.
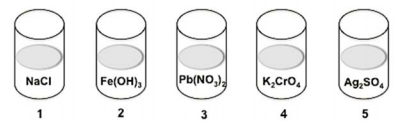
Gotejando solução de HCl 1M sobre cada uma dessas cinco soluções, haverá a formação de precipitado somente nos frascos
Observe a equação química a seguir.
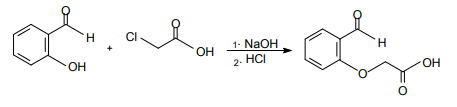
O produto formado é um composto que apresenta os grupos funcionais característicos das funções orgânicas
A estocagem de sódio metálico deve ser feita em frasco contendo, geralmente, hexano ou querosene que deve estar bem fechado para evitar o contato com a umidade do ar atmosférico. Isso porque o sódio metálico é capaz de
Se um composto químico fortemente oxidante for guardado próximo a composto químico inflamável e se houver danificação das embalagens ou volatilização e eles entrarem em contato, existe uma probabilidade bastante elevada de ocorrer incêndio ou explosão. Desse modo, ao guardar ou estocar produtos químicos deve-se evitar a proximidade de embalagens contendo soluções concentradas de
Uma amostra de Acetanilida (N-feniletanoamida) foi pesada em balança analítica com precisão de ±0,00001, e o valor encontrado foi 9,56243 gramas. Se for pesada em outra balança, com precisão ±0,001, a massa de Acetanilida, em gramas, deverá ser expressa como
Observe o esquema abaixo.
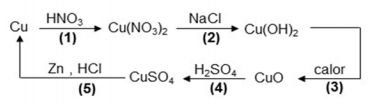
O esquema representa de forma abreviada as reações químicas do ciclo do cobre. As etapas em que o cobre é, respectivamente, oxidado e reduzido são as
O ácido 2,3-dibromossuccínico pode ser obtido em laboratório por meio da reação do ácido fumárico com bromo, em meio aquoso, como representado na equação química
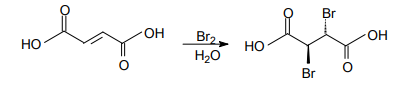
O mecanismo dessa reação é denominado
Com base nas seguintes informações, responda a questão.
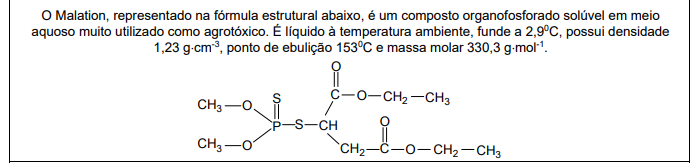
Com base nas propriedades apresentadas, é correto afirmar que esse composto
Após as manipulações cotidianas em um laboratório de química, o técnico lavou a vidraria utilizada e a colocou na estufa para secagem. O técnico errou se colocou na estufa
O descarte incorreto de resíduos químicos pode causar sérios danos aos indivíduos e ao meio ambiente.
Sendo assim, não se deve(m) descartar, na pia do laboratório,
Observe o esquema abaixo.
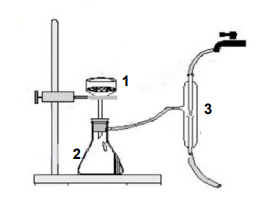
Nesse esquema os utensílios de laboratório indicados por 1, 2 e 3 são denominados, respectivamente,
Uma amostra de sulfato cúprico hidratado pesando 125,2 g foi seca em estufa a 110°C para remover toda a água de hidratação. Após a secagem, a amostra pesou 80,0 g. Então a fórmula do sal hidratado em questão é
Trifluoreto de boro reage com boridreto de sódio e produz tetrafluorborato de sódio e diborano, que, ao reagir com o oxigênio do ar, produz óxido de boro e água, como representado nas equações químicas não balanceadas:
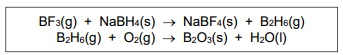
Partindo-se de 111 gramas de boridreto de sódio e considerando que este é o reagente limitante e, ainda, que o rendimento da reação é 90%, a massa, em gramas, de óxido de boro produzido será
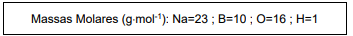
Com base nas seguintes informações, responda a questão.

O teor (%) de fósforo em um mol desse composto é de aproximadamente,


