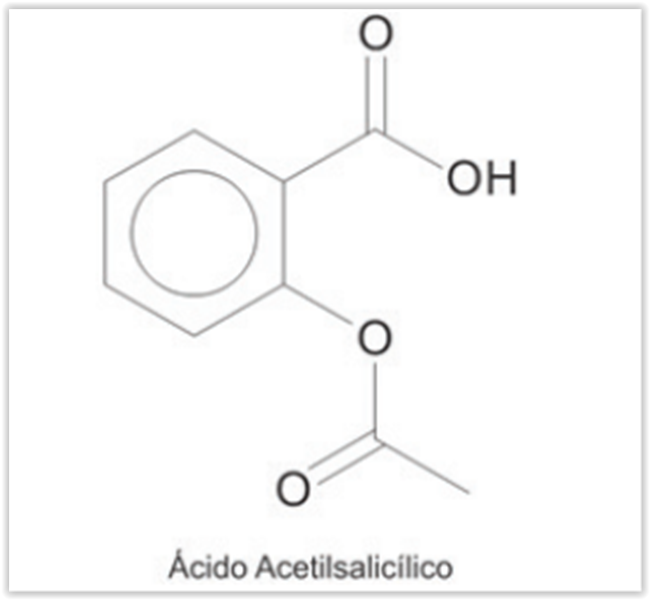
Na análise volumétrica de 0,5 g de uma amostra de
medicamento constituído por ácido acetilsalicílico
(AAS), foram utilizados 15 mL de hidróxido de sódio com
concentração 0,01mol/L Considerando que a reação
com a base ocorre apenas para o ácido acetilsalicílico,
não tendo participação das outras substâncias reativas
na amostra, qual a porcentagem de AAS presente no
fármaco analisado? Dados: M (AAS) = 180,16g/mol
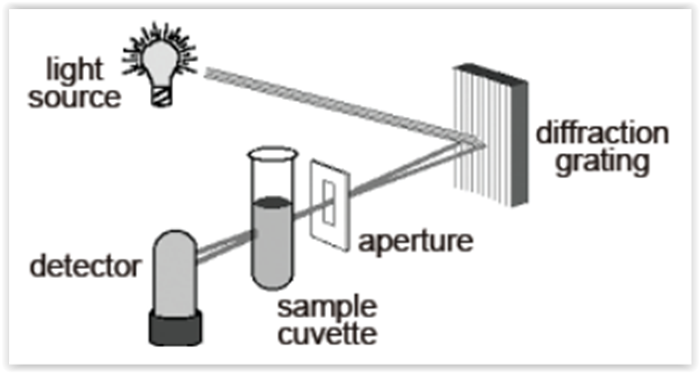
A figura a seguir apresenta um esquema simplificado
de um equipamento de espectrofotometria de absorção
molecular, analise as propostas apresentadas:
I.A rede de difração seleciona o comprimento de onda
para se proceder na investigação, porém a seletividade
do sistema está relacionada com a abertura da fenda
de passagem de luz, quanto menor a fenda, mais
específico será o comprimento de onda selecionado.
II.Absorbância está relacionada com a intensidade de luz
visível que a amostra absorveu, sendo que se a cubeta
apresentar maior ou menor caminho óptico o sinal de
absorbância permanece o mesmo, já que a solução não
foi alterada.
III.Soluções muito concentradas podem causar um
bloqueio da luz incidente ao passar pela cubeta, fora
da proporcionalidade, com isso ocorre um desvio
de linearidade, além disso, este sistema também é
prejudicado por material particulado ou manchas na
superfície da cubeta.
São verdadeiras:
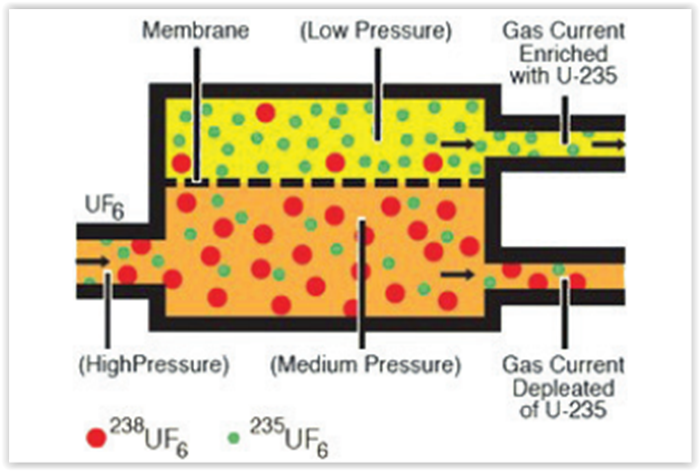
Uma das etapas de enriquecimento do urânio consiste
na separação do hexafluoreto de urânio, contendo U-235
do U-238, analise o esquema representado a seguir:
I.Ocorre redução da pressão do sistema naturalmente,
pois na linha de entrada da mistura de gases, ocorre
uma expansão na chegada a câmara de difusão em
membrana.
II.A introdução de um sistema de vácuo na linha do U -235
enriquecido favorece a maior velocidade da separação
dos componentes do sistema.
III.A difusão do composto contendo U-238 pela membrana
é mais intensa, por isso é necessário reduzir a pressão
do sistema garantindo assim a maior passagem pela
membrana do composto contendo U – 235.
São verdadeiras as afirmações contidas na alternativa:
O espinafre é uma planta de interesse nutricional
constituída principalmente de dois grupos de
moléculas os carotenóides e as clorofilas. A técnica da
cromatografia em coluna é importante no processo de
isolamento dessas substâncias. Após uma preparação
conveniente, o extrato do espinafre é adicionado
à coluna cromatográfica, onde uma das moléculas
têm mais afinidade ao sulfato de cálcio (CaSO4) que
constitui a coluna. É adicionado hexano que arrasta a
primeira banda. Ao se mudar a fase móvel para acetona,
retira-se as moléculas que mais interagiram com a fase
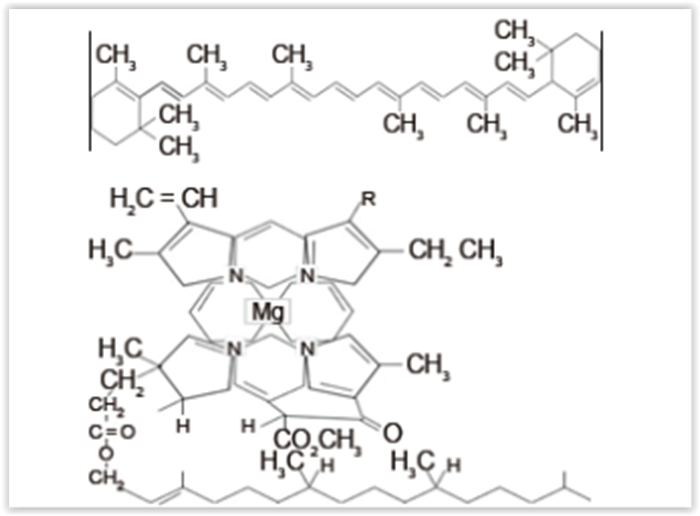
estacionária, formando a segunda banda. Abaixo se
encontram as fórmulas estruturais das duas moléculas
principais que constituem o extrato de espinafre e que
podem ser retiradas pelo procedimento descrito:
Com base nos seus conhecimentos sobre LC, no texto
e nas estruturas das moléculas assinale o que está
correto:
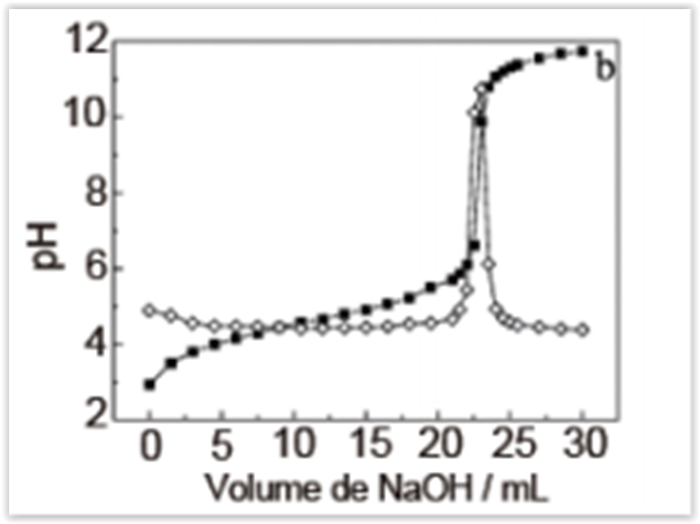
A figura a seguir apresenta duas curvas quase
que sobrepostas, correspondentes ao mesmo
procedimento: a curva de titulação entre um fármaco
ácido e NaOH e a curva obtida quando se tira a 1ª
derivada da curva de titulação. Analise as afirmações e
escreva V para verdadeiro ou F para falso:
( ) A titulação envolve ácido fraco e base forte, se não fosse potenciométrica a utilização de fenolftaleína como indicador, teria
preferência a utilização de alaranjado de metila.
( ) O p.e. (ponto de equivalência) será em pH igual 7.
( ) o pKa do titulado é próximo a 5.
( ) A derivada da curva tem por finalidade indicar o volume
gasto até o p.e. para a neutralização.
( ) O sitema atua como um tampão na faixa 4
Um estudante pretende preparar uma solução 2,0 mol L-1 a partir do ácido clorídrico concentrado. Ao abrir um manual elaborado por estudantes do Ensino Médio se deparou com as seguintes afirmações: I.“Realizem o procedimento na bancada do laboratório, utilizando avental, óculos de segurança e luvas.” II.“Retirem uma alíquota do ácido clorídrico concentrado vertendo-a em um béquer, pipetem o volume necessário a partir do béquer e transfira o volume para o balão volumétrico e adicionem água até o menisco e agitem.” III.“Despejem cuidadosamente o volume pipetado de ácido clorídrico concentrado na água.” IV.“Evite o contato dos vapores do ácido clorídrico com olhos e mucosas, lavando a mão com água ao término do procedimento.” É correto apenas o que se afirma em:
Dois recipientes idênticos chamados 1 e 2, contém respectivamente, 64 g de SO2 (M = 64g/mol) à pressão P1 e temperatura de 27 ºC e 64 g de O2 (M = 32g/mol) à pressão P2 e temperatura 327 ºC. Comparando-se as pressões dos gases, tem-se:
A análise quantitativa por espectrofotometria UV/Visível
é muito utilizada para doseamento de determinados
princípios ativos e corantes em formulações
farmacêuticas disponíveis no mercado. Essa análise é
confiável desde que obedeça a Lei de Beer, ou seja, a
solução analisada deve obrigatoriamente seguir uma
relação linear entre a absorbância e a concentração.
Considere a análise de um determinado fármaco
que obedece a Lei de Beer. O que aconteceria com o
valor de Absorbância se a concentração da solução
do fármaco fosse o dobro? Considere que para esta
análise utilizou-se uma cubeta de 1,00 cm de caminho
óptico. O que aconteceria com o valor de Absorbância
se uma nova medida fosse realizada com uma cubeta
de 5,00 cm de caminho óptico?
Um medicamento à base de ferro pode ter sua
concentração conhecida por espectrofotometria UV/
Visível. Utilizando-se um medicamento de referência,
realizaram-se as devidas diluições para a construção de
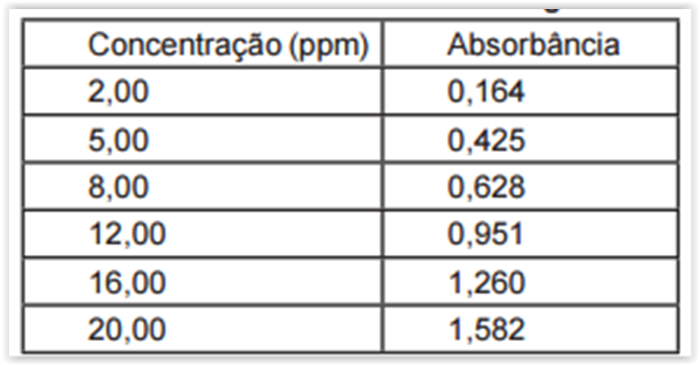
uma curva de calibração. As medidas de absorbância,
no comprimento de onda de absorção máxima de 510
nm, nas diferentes concentrações do medicamento de
referência encontram-se na tabela a seguir:
Os dados obtidos permitiram a construção de uma
curva de calibração com coeficiente de correlação (R²)
de 0,99978 e equação da reta: A = 0,01478 + 0,07812
x C. Sabendo-se que a absorbância da solução do
medicamento à base de ferro foi de 0,715. Analise as
propostas:
I.A concentração da amostra analisada é de 8,96 ppm.
II.O analito deve ser colorido, pois o comprimento de onda é na região do visível.
III.A absorbância está relacionada diretamente com a
quantidade de radiação que atravessou a amostra
analisada.
IV.A curva de calibração construída não se mostrou linear
para o trecho estudado.
V.Se a amostra apresentar um valor de absorbância de
1,782 a concentração será de 22,60 ppm.
São corretas:
A irradiação de alimentos e medicamentos tornouse
prática importante para ampliar a durabilidade
destas substâncias. Expostas às radiações beta e
gama, as substâncias que passam por este processo
apresentam, além da esterilização, manutenção da sua
aparência física e qualidades de sabor.
Analise as proposições a seguir:
I.Um alimento irradiado pode contaminar os demais em
um centro de distribuição, com isso há necessidade de
embalagens adequadas para evitar contaminações por
contato.
II.Os bombardeadores de césio e cobalto são fontes
emissoras das radiações beta e gama, ao irradiar uma
amostra alimentícia ou medicinal, o material torna-se
radioativo por um certo tempo, necessitando de repouso
até que transcorra algumas meia-vidas antes de seguir
para o centro de distribuição.
III.Apesar de alimentos irradiados serem comuns, não
existe uma “dose de pasteurização" definida para cada
um deles, pois são tratados de forma empírica um a um.
Assinale a alternativa que contenha apenas proposições
verdadeiras:
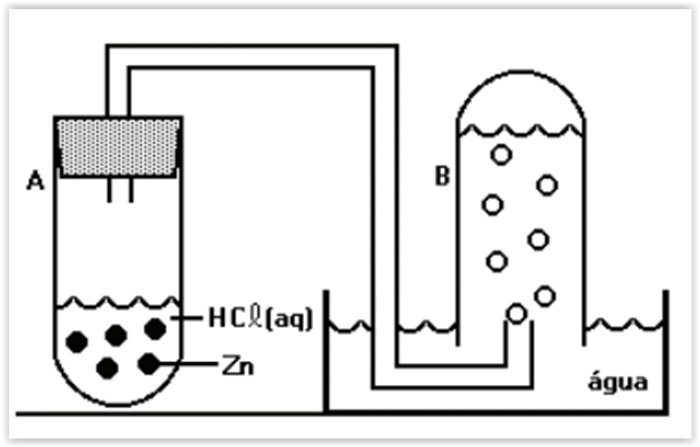
Um tubo inicialmente cheio de água (B ) foi conectado a
outro tubo (A ), ao qual foi adicionada solução de ácido
clorídrico e raspas de zinco com alto grau de pureza. O
sistema foi fechado e após algum tempo, apresentavase
como indicado na figura.
Analise as propostas a seguir:
I.Parte significativa do gás hidrogênio ficará retida na
água formando uma solução de caráter ácido.
II.A pressão de vapor da água, na temperatura da
realização do experimento, é importante para o cálculo
sobre o volume de hidrogênio, caso não se leve em
consideração a pressão de vapor da água o valor de
gás hidrogênio obtido será maior que o verdadeiro.
III.Quando o nível da água no interior do tubo B se igualar
com o nível da água do restante da cuba, pode-se
afirmar que a soma da pressão do hidrogênio com a
pressão de vapor da água, na temperatura de realização
do experimento, será praticamente igual à pressão
atmosférica local.
Assinale a alternativa que contém as propostas
verdadeiras:
O ácido perclórico P.A. apresenta concentração de 70%, sabendo que a densidade do ácido perclórico é 1,68g/cm-3 , assinale a alternativa que apresente o volume aproximado de solução do ácido que deve ser adicionado a um balão volumétrico de 200mL, afim de preparar uma solução 0,1 mol/L. Dados M=100,46g.mol-1
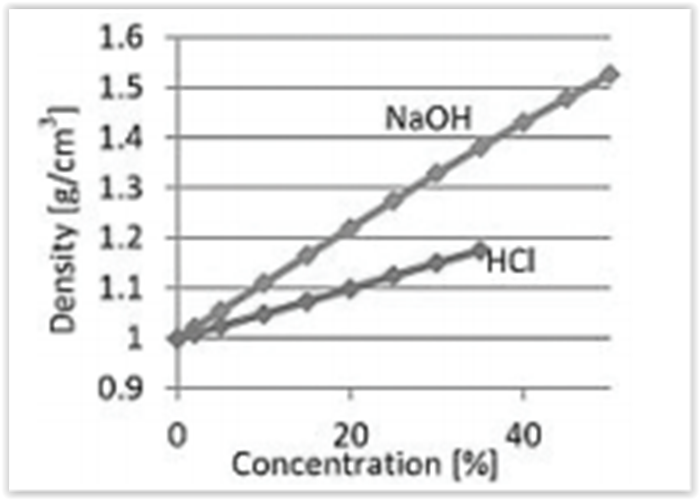
O diagrama a seguir apresenta a relação entre a
densidade e a concentração em porcentagem em
massa para o hidróxido de sódio (M = 40 g/mol) e o
ácido clorídrico (M = 36,5 g/mol).
Em uma situação hipotética, onde as duas soluções
apresentem densidade ao redor de 1,1g/cm³
é correto
afirmar que as concentrações, em mol/L, para o NaOH e
para o HCl serão respectivamente:
Um cilindro contém uma mistura de 88 g de CO2
(g)
com uma quantidade desconhecida de gás argônio
foi mantido em determinadas condições de pressão e
temperatura.
Depois de vários testes, descobriu-se que com a adição
de 220g de CO2
(g) à mistura, mantendo-se temperatura
e pressão constantes, o volume dobra.
Assinale a alternativa que apresenta a quantidade de
argônio existente na mistura.
Dados: Massa atômica: Ar=40u; C=12u; O=16u
A constituição da matéria está presente no vocabulário
científico desde a Grécia antiga, mas sem comprovação
científica, apenas filosófica. Como conhecimento
científico os modelos atômicos foram formulados a
partir de 1808 e à medida que novos e melhores métodos
de investigação foram sendo desenvolvidos, evoluídos.
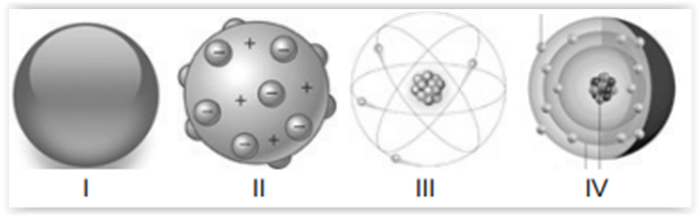
A seguir, são apresentadas as representações gráficas
de alguns modelos atômicos:
Julgue os itens a seguir:
( ) Dalton, figura I, tomou como base para o desenvolvimento
de seu modelo atômico análises de conservação e
proporcionalidade da massa em uma reação, originárias
de Lavoisier e Proust.
( ) O modelo atômico de Thomson , figura II, apresenta a
ideia de descontinuidade pela primeira vez e apresenta
a primeira subpartícula atômica encontrada: o elétron.
( ) A figura III representa o modelo atômico de Rutherford,
destacando o surgimento da ideia de núcleo positivo,
sem os nêutrons que só seriam descobertos por
Sommerfeld em 1932.
( ) A figura IV representa o átomo de Chadwick, organizando
os níveis de energia eletrônicos pela primeira vez.
Assinale a alternativa que contém a análise correta em
verdadeiro ( V) e falso (F ) para os itens apresentados.