O gás nitrogênio (N2) é o que se encontra em maior proporção no ar atmosférico. Por ser considerado um gás inerte, ele pode estar presente em diversos processos laboratoriais e industriais. Sua obtenção é feita através da liquefação fracionada do ar atmosférico. Supondo que, a partir desse processo, obteve-se uma amostra de 280g desse gás, é correto afirmar que o volume ocupado por ele sob condições normais de temperatura e pressão foi de
Dado: MMN = 14 g/mol
O potencial químico de um gás perfeito é uma função linear do logaritmo da pressão. Porém, para gases reais, esta linearidade não se verifica. Que conceito termodinâmico é utilizado para compensar esse desvio da idealidade visando manter a linearidade e um formalismo semelhante?
200 g de hidrogênio molecular (H2) em condições de gás real são colocados em um cilindro de raio 50 cm e altura 100 cm. A temperatura interior do cilindro é – 182° C. A pressão deste gás no sistema, nestas condições, será aproximadamente
(Dados: PM: H=1,0 g/mol; R=0,08206 atmL/molK; a=0,244 L² atm/mol² ; b=0,02661 L/mol.)
O gás amônia, perigoso aos seres humanos, é de uso comum nas indústrias alimentícias, petroquímicas e metalúrgicas com várias aplicações. Mesmo exigindo o uso adequado de equipamentos de proteção individual e procedimentos de segurança, uma indústria teve o gás amônia recentemente citado em um vazamento de gás que levou centenas de seus funcionários a procurar atendimento médico com sintomas característico de intoxicação. A respeito da produção do gás amônia apresentado na equação a seguir, assinale a alternativa que apresenta o volume do gás NH3 obtido a partir de 12 L de N2(g).
Considere todos os gases nas condições normais de temperatura e pressão (CNTP).
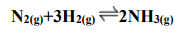
Um técnico do laboratório de Química do IFTO deseja identificar o conteúdo de um cilindro contendo um gás monoatômico puro. Para isso, coletou uma amostra do gás e determinou sua densidade (d=5 g/L), a 27 °C e 1 atm. Assumindo o modelo do gás ideal e empregando as informações anteriores, é possível estimar que a massa molar do gás vale:
Adotar nessa questão: R = 0,082 atm.L. mol-1 . K-1; T( K ) = 273 + T(°C)

Considere as reações I, II e III a seguir.
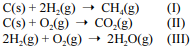
Com relação a essas informações, julgue o item que se segue.
De acordo com as leis das reações gasosas de Gay Lussac, sob mesma temperatura e pressão, o volume ocupado pelo CO2 é maior que o volume do O2 na reação II.
O ar atmosférico é formado por vários componentes, incluindo vários gases, vapor d'água, micro-organismos e impurezas. O gás mais abundante presente no ar atmosférico é:
Sobre as propriedades dos gases ideais, julgue as sentenças a seguir:
I. O volume de um gás, à temperatura constante, diminui com o aumento da pressão.
II. O aumento da temperatura de um gás, à pressão constante, causa diminuição do volume do gás.
III. Um processo termodinâmico que ocorre a volume constante é chamado de processo isocórico.
Está(ão) correta(s) a(s) sentença(s):
Sejam as propriedades massa (M), índice de Wobbe (Wo), e poder calorífico superior (P ) (este último em kJ/m3 ); e os subscritos DEST representando destino e ORIG, origem. No transporte do GNL por navios, o não isolamento total leva à vaporização e à perda de certa quantidade de material. Sendo o GNL composto por uma mistura de hidrocarbonetos, admitindo-se que a densidade não sofra variações muito significativas, a carga líquida que chega ao destino apresenta
A Lei de Efusão de Gases, escrita por Graham em 1846, afirma:
“a velocidade de efusão de um gás é inversamente proporcional à
raiz quadrada de sua densidade,ou de seu peso molecular."
A velocidade de um gás hipotético X2, através de um orifício,
corresponde a 0,315 vezes à velocidade do gás hidrogênio (H2),
formado apenas por isótopos de número de massa 1,0 através do
mesmo orifício nas mesmas condições de temperatura e pressão.
O valor do número de massa de X determinado pela Lei de
Graham é aproximadamente:
Dado: √ = 1,414
A seguir tem-se a definição de uma grandeza físico-química:
“É decorrente das colisões das moléculas de um gás com a parede do recipiente que o contém."
Qual opção apresenta a grandeza definida?

